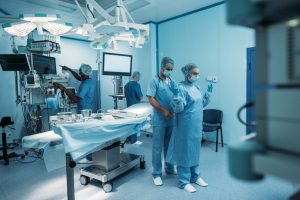
Rumah Sakit Chicago USA Tempat Penelitian Mikroorganisme
Rumah Sakit Chicago USA Tempat Penelitian Mikroorganisme – Pada masa kini berbagai tempat digunakan untuk meneliti berbagai mikroorganisme untuk berbagai keperluan. Perkembangan berbagai tempat seperti rumah sakit dan universitas untuk menjadi pusat penelitian ini bukanlah sesuatu yang terjadi begitu saja tapi merupakan sesuatu yang terjadi secara perlahan dan sesuai dengan perkembangan teknologi terbaru. Rumah sakit Chicago USA merupakan salah satu tempat yang biasa dijadikan andalan di Amerika untuk melakukan berbagai macam percobaan dan penelitian mengenai berbagai bakteri atau secara khusus bekerja untuk meneliti mikroorganisme yang menyebabkan penyakit. Berbagai macam penelitian sudah dilakukan pada tempat ini untuk menemukan penyebab, cara penyebaran, dan cara menangkal berbagai macam virus dan bakteri yang menyebabkan penyakit.
Salah satu fokus penelitian yang biasa dilakukan di rumah sakit ini adalah tentang ekologi. Ekologi dapat dikatakan sebagai sebuah ilmu khusus yang bertujuan untuk mempelajari interaksi organisme dengan organisme lain. Berbagai penelitian telah dilakukan untuk mengetahui pengaruh bakteri tertentu terhadap makhluk hidup paling di sekitarnya. Penelitian ini memiliki banyak manfaat untuk mengenal berbagai bakteri dan mikroorganisme lain, mencari manfaat dan mengetahui bahaya dari makhluk tersebut terhadap lingkungan sekitarnya. Dari penelitian ini akan muncul berbagai macam solusi untuk berbagai hal. Misalnya cara untuk mempertahankan makanan agar bisa bertahan lebih lama. Makanan menjadi fokus yang sering dibahas karena pada berbagai tempat makanan bisa menjadi mudah basi. Memahami interaksi bakteri dengan makanan dapat membuat berbagai jenis makanan bisa disimpan dengan baik dalam jangka waktu yang lebih lama.
Seiring berjalannya waktu bahan makanan akan semakin sedikit karena kemampuan produksi makanan pada akhirnya tidak akan seimbang dengan manusia yang akan memakannya. Di berbagai tempat pada saat ini sudah terjadi kelangkaan makanan sehingga banyak orang yang memakan-makanan sintetis atau makanan yang sudah tidak layak. Untuk menjaga daya tahan makanan berbagai macam teknologi diterapkan pada berbagai alat penyimpanan makanan sehingga pertumbuhan bakteri dapat dihambat.
Bakteri yang memiliki fungsi sebagai makhluk yang membantu proses pembusukan juga mengalami perkembangan. Pada saat ini sudah banyak jenis bakteri yang menghasilkan efek pembusukan. Beberapa jenis bakteri berasal dari perkawinan dan mutasi yang tidak semestinya sehingga menghasilkan jenis bakteri baru yang memberikan efek lebih besar pada penguasaan bahan makanan. Rumah Sakit Chicago USA tidak hanya melakukan penelitian tapi juga menyimpan berbagai hasil penelitian dari seluruh dunia sehingga sudah banyak data tersimpan mengenai berbagai macam bakteri dan perubahannya yang telah diteliti orang.

Penelitian bakteri yang dilakukan oleh salah satu anggota agen bola yang menjadi seorang peneliti terkenal merupakan sesuatu yang sangat bermanfaat bagi kehidupan manusia dan selama manusia hidup mereka akan selalu berinteraksi dengan bakteri. Tidak semua bakteri berbahaya untuk kesehatan karena di dalam tubuh manusia terdapat berbagai macam jenis bakteri yang memiliki efek tersendiri pada tubuh sehingga dapat mempengaruhi pertumbuhan dan pencernaan di dalam tubuh manusia. Bakteri ini sering disebut dengan probiotik yang terdiri dari banyak macam bakteri dengan berbagai fungsi. Walaupun penelitian mengenai hal ini sudah dilakukan sejak lama tapi masih belum semua bakteri diketahui dengan jelas interaksi dan fungsinya.
Memiliki peralatan yang memadai untuk melakukan penelitian bakteri merupakan salah satu keunggulan dari Rumah Sakit Chicago USA. Berbagai akademisi yang memang ahli di bidang ini bekerja untuk mencari berbagai penemuan baru mengenai berbagai macam bakteri dan interaksi bakteri ,dengan lingkungannya dengan tujuan untuk memberikan kualitas hidup yang lebih baik untuk seluruh umat manusia.
Penelitian Tentang Seberapa Pentingkah Mikroorganisme?
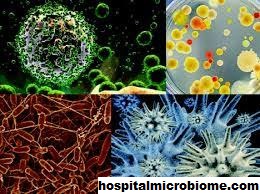
Penelitian Tentang Seberapa Pentingkah Mikroorganisme? – Mikroba adalah bagian integral dan esensial dari jaring kehidupan. Mereka melakukan berbagai fungsi ekologis yang penting, mulai dari mendaur ulang bahan organik hingga membantu siklus karbon dan nitrogen.
Penelitian Tentang Seberapa Pentingkah Mikroorganisme?
hospitalmicrobiome – Artikel ini akan membahas pentingnya mereka bagi alam dan industri manusia dan masyarakat serta aplikasinya di beberapa industri utama.
Baca juga : Kehidupan Ekologi Mikroba Yang Sangat Beragam
Manusia dan mikroba: Sejarah singkat
Melansir news-medical, Penyakit yang disebabkan oleh mikroorganisme patogen telah menjadi pembunuh utama sepanjang sejarah. Kelangsungan hidup spesies kita yang berkelanjutan telah menjadi sumber daya tarik bagi orang-orang sejak zaman prasejarah. Selama ribuan tahun, dokter dan ilmuwan telah berjuang untuk lebih memahami penyakit telah menyebabkan banyak perawatan, beberapa sayangnya tidak seefektif yang lain. Domestikasi hewan untuk sumber makanan juga membawa masalah tambahan, dengan patogen melompat dari hewan ke inang manusia.
Manusia telah memiliki hubungan intim dengan mikroba sepanjang sejarah, menggunakannya untuk banyak tujuan penting. Industri makanan terutama telah lama menggunakan mikroba, dan selama beberapa abad terakhir mereka telah digunakan dalam ilmu kehidupan dan industri medis, industri energi, pengolahan limbah, dan banyak lagi industri lainnya.
Mikrobiologi, studi tentang mikroba, telah ada sejak awal abad ke-17 dengan penemuan mikroskop. Karya-karya sebelumnya seperti teori penyakit menular pada abad ke-16 , yang dikemukakan oleh Girolamo Fracastoro, membuka jalan bagi bidang tersebut. Studi modern telah mengungkapkan rincian lebih lanjut tentang struktur dan penggunaan mikroorganisme seperti virus, bakteri, jamur, dan plasmodia.
Ribuan produk industri penting berasal dari mikroba termasuk actinomycetes, bakteri, dan jamur. Lebih banyak produk yang dibuat oleh ahli mikrobiologi memasuki pasar setiap tahun.
Mikroorganisme di alam
Mikroorganisme memainkan peran intrinsik di hampir setiap siklus alam. Ditemukan di sebagian besar lingkungan, dari perairan hingga darat, udara, di dalam tubuh manusia, dan bahkan di lingkungan ekstrem seperti ventilasi hidrotermal dan gunung berapi, mikroorganisme merupakan bagian penting dari jaring kehidupan.
Mikroba membantu memecah bahan organik dari tumbuhan, hewan, dan mikroba lainnya. Mereka terlibat dengan siklus nitrogen dan karbon. Mikroorganisme membantu menghasilkan oksigen dan karbon dioksida, serta memperbaiki nitrogen atmosfer menjadi bentuk yang dapat digunakan untuk banyak organisme. Mereka juga membantu hewan menelan makanan dengan menjadi bagian dari mikrobioma usus. Beberapa spesies mikroba bersimbiosis di alam. Diperkirakan jumlah total bakteri dan archaea di Bumi berada di kisaran 10 30 .
Mikroba dan penemuan obat
Mikroorganisme menyebabkan berbagai penyakit pada manusia, tumbuhan, hewan, dan bahkan ada strain mikroba (seperti bakteriofag) yang bersifat patogen bagi mikroorganisme lain. Kemajuan awal di bidang kedokteran yang memanfaatkan mikroba antara lain penemuan penisilin dan pengembangan antibiotik pada awal abad ke- 20 dan penemuan vaksin yang efektif melawan cacar pada abad ke- 19.
Mikroba digunakan dalam berbagai studi penemuan obat saat ini. Pada tahun 1991, setengah dari obat-obatan yang ada di pasaran adalah produk alami atau turunannya. Pada tahun 1997, 42% dari obat-obatan terlaris diperoleh dari sumber alami. Saat ini, ratusan ribu metabolit sekunder telah diidentifikasi, dan ini digunakan secara luas dalam industri farmasi. Antivirus, antibiotik, dan antijamur biasanya digunakan dalam pengaturan perawatan kesehatan di seluruh dunia.
Resistensi terhadap obat telah berkembang dalam beberapa dekade terakhir, terutama resistensi antibiotik. Ini menghadirkan beberapa tantangan dalam penemuan obat, tetapi obat desainer baru memasuki pasar yang memungkinkan dokter untuk mengobati dan menyembuhkan penyakit mematikan yang semakin sulit diatasi melalui cara yang ada.
Mikroba dalam industri makanan
Sejarah penggunaan mikroba dalam industri makanan dimulai dari jaman dahulu. Banyak produk makanan termasuk roti, yogurt, keju, kombucha, daging yang diawetkan dan diawetkan, dan minuman beralkohol memanfaatkan mikroba dan reaksi kimianya. Mikroba juga memainkan peran penting dalam usus sebagai bagian dari mikrobioma, yang telah mendorong teknik untuk meningkatkan desain makanan ramah mikrobioma.
Teknik untuk mencegah kontaminasi oleh bakteri patogen meningkatkan keamanan pangan, desain, kualitas, dan umur simpan. Kemasan makanan antimikroba adalah teknologi yang relatif baru dikembangkan dalam industri makanan. Penelitian tentang mikroba dan perlindungan terhadap bahayanya bagi kesehatan manusia adalah sangat penting bagi industri makanan bernilai miliaran dolar.
Pengolahan limbah dan perbaikan lingkungan
Mikroba memecah dan memakan kotoran manusia. Mereka telah digunakan dalam pengolahan limbah dan air limbah selama beberapa abad terakhir, dengan aplikasi yang semakin canggih meningkatkan sanitasi dan kesehatan untuk miliaran orang di seluruh dunia. Bakteri aerob dan anaerob umumnya dimanfaatkan oleh industri limbah.
Penelitian selama beberapa dekade terakhir juga telah menyediakan aplikasi mikroba untuk membersihkan polusi dan membuang sampah plastik, dua masalah paling kritis yang dihadapi masyarakat modern. Sistem mikroba yang membantu mengurangi emisi karbon juga telah dieksplorasi secara ekstensif.
Mikroba dan pertanian
Pertanian mengambil keuntungan dari siklus alami dan perilaku tumbuhan dan hewan. Mikroba telah memainkan peran penting dalam sejarah pertanian dan pertanian. Mereka adalah sumber perhatian utama bagi petani dan ilmuwan pertanian karena penyakit umum seperti busuk hitam, busuk lunak bakteri, bercak daun bakteri, hawar, dan berbagai infeksi jamur dan virus yang mempengaruhi tanaman di seluruh dunia. Banyak perawatan dan strategi remediasi telah dikembangkan selama bertahun-tahun.
Perkembangan penting baru-baru ini di bidang pertanian adalah modifikasi genetik. Teknik modifikasi genetik menggunakan mikroba untuk mengamplifikasi gen yang menguntungkan. Munculnya modifikasi genetik, meskipun kontroversial, menawarkan kemungkinan tanaman dan galur tahan penyakit yang menunjukkan respons yang lebih kuat terhadap perubahan iklim. Mikroba secara intrinsik terkait dengan masa depan pertanian berkelanjutan.
Masa depan
Banyak teknologi inovatif yang memanfaatkan mikroba saat ini. Mereka saat ini sedang dieksplorasi untuk konstruksi, bioremediasi, keamanan dan pembangkitan energi, dan banyak lagi. Masa depan hubungan kita dengan organisme yang penting secara industri ini kemungkinan akan sama rumit dan menariknya dengan sejarah panjang kita dengan mikroorganisme.
Cara mendaftar uji coba vaksin COVID-19 di UChicago Medicine
hospitalmicrobiome – University of Chicago Medicine telah meluncurkan pendaftaran bagi individu untuk berpartisipasi dalam uji coba fase 3 vaksin untuk melawan virus penyebab COVID-19.
Cara mendaftar uji coba vaksin COVID-19 di UChicago Medicine – Individu dapat bergabung dengan pendaftaran UChicago Medicine untuk berpartisipasi dalam uji coba vaksin ini dan dalam penelitian pencegahan COVID-19 di masa mendatang.
Cara mendaftar uji coba vaksin COVID-19 di UChicago Medicine
Pusat Medis Universitas Chicago adalah tempat pengujian vaksin Moderna. Ini juga akan menjadi situs pengujian untuk studi penelitian klinis Fase 3 Janssen Pharmaceutical Companies of Johnson & Johnson, uji coba ENSEMBLE, untuk mengevaluasi keamanan dan kemanjuran kandidat vaksin COVID-19 yang diteliti Janssen, JNJ-78436735, juga dikenal sebagai Ad26. COV2.S.
Uji coba Janseen adalah uji klinis acak fase 3, double-blind, terkontrol plasebo, yang dirancang untuk mengevaluasi keamanan dan kemanjuran dosis vaksin tunggal kandidat vaksin Janssen COVID-19 versus plasebo. Seluruh penelitian direncanakan untuk mencakup sekitar 60.000 orang dewasa berusia 18 tahun ke atas, termasuk perwakilan signifikan dari mereka yang berusia di atas 60 tahun.
UChicago Medicine akan mendaftarkan hingga 2.000 orang dewasa berusia 18 tahun ke atas dari dalam komunitas Chicago. Studi ini akan mencakup mereka yang memiliki dan tanpa penyakit penyerta yang terkait dengan peningkatan risiko COVID-19 yang parah.
Baca Juga : Rumah Sakit Chicago Dapatkan Grade A untuk Keselamatan Pasien
Bagian dari komunitas
Partisipasi UChicago Medicine dalam uji klinis nasional berskala besar ini penting karena lokasi rumah sakit dan koneksi ke komunitas South Side. Sementara ribuan calon sukarelawan telah mendaftar untuk dipertimbangkan untuk uji coba vaksin di wilayah Chicago, para peneliti di UChicago berharap dapat meningkatkan representasi orang kulit berwarna dan kelompok tertentu dari pasien berisiko, termasuk orang tua dan mereka yang memiliki penyakit kronis seperti seperti diabetes, hipertensi, dan penyakit jantung.
“Kami tahu bahwa pasien Afrika-Amerika dan Hispanik secara tidak proporsional dipengaruhi oleh COVID-19, dan kami ingin memastikan bahwa orang-orang dari semua ras terwakili dalam uji coba penting ini. Kami berharap anggota komunitas di sekitar University of Chicago akan secara sukarela berpartisipasi,” kata David Pitrak, kepala Bagian Penyakit Menular di UChicago Medicine.
“Sangat penting untuk memiliki perwakilan yang memadai dari semua ras dan etnis dalam uji klinis untuk memastikan bahwa vaksin seefektif mungkin untuk sebanyak mungkin orang. Dan kami benar-benar ingin dapat menawarkan vaksin kepada mereka yang berisiko tinggi.”
Uji coba ini merupakan bagian dari uji coba nasional besar yang berusaha untuk mendaftarkan ribuan peserta. Pasien akan dipantau setelah suntikan untuk menentukan apakah vaksin dapat mencegah gejala COVID-19. Peserta akan dilacak selama 27 bulan.
“Pertanyaan utama seputar vaksin ini dan semua vaksin SARS-CoV-2 bukan hanya apakah vaksin tersebut dapat menginduksi respons imun tetapi seberapa tahan lama respons imun terhadap vaksin?” kata Kathleen Mullane, direktur uji klinis penyakit menular di UChicago Medicine. “Itulah mengapa studi akan berlangsung selama dua tahun. Kami tahu bahwa vaksin yang masuk ke uji coba fase 3 dapat menghasilkan respons imun, tetapi kami tidak tahu berapa lama respons itu akan bertahan atau apakah pasien akan memerlukan suntikan booster tahunan, seperti yang mereka lakukan dengan influenza.”
Habibul Ahsan, direktur Institute for Population and Precision Health di UChicago Medicine, mencatat bahwa pemantauan pasca-vaksinasi akan mencakup tes darah untuk menentukan tingkat antibodi dan persistensi antibodi dari waktu ke waktu, serta kontak mingguan dengan sukarelawan untuk melacak apakah peserta sakit.
Mereka yang mengalami gejala COVID-19 akan dites virusnya dengan cepat. Data ini akan membantu menentukan apakah vaksin melindungi terhadap tertular virus dan apakah vaksinasi dapat mengurangi keparahan gejala jika seseorang menjadi sakit.
Mencari basis sukarelawan yang luas
Karena Operation Warp Speed bertujuan untuk menghasilkan 300 juta dosis vaksin yang disetujui pada bulan Januari, sangat penting bagi uji klinis untuk merekrut dan mendaftarkan peserta dari segala usia dan latar belakang ras.
Tanpa data yang memadai yang mencerminkan populasi minoritas dan berisiko tinggi, para peneliti tidak dapat memastikan bahwa vaksin itu efektif dan aman untuk semua pasien yang berisiko tertular virus. UChicago Medicine berencana untuk bekerja dengan basis komunitasnya yang sudah kuat untuk memastikan bahwa pendaftaran dalam studi penting ini mewakili kelompok minoritas di wilayah Chicago.
Para peneliti akan merekrut peserta di lingkungan rumah sakit, serta di masyarakat, dalam beberapa kasus menggunakan unit medis keliling yang akan membawa vaksin ke pintu depan orang-orang. “Kami ingin mempermudah para sukarelawan untuk berpartisipasi dalam penelitian ini, dan kami ingin memastikan bahwa komunitas yang dilayani rumah sakit kami terwakili dengan baik dalam uji coba ini,” kata Dr. Ahsan.
Dengan data keamanan dan respons imun yang menjanjikan dari uji coba fase 1 dan 2 untuk vaksin ini, para peneliti bersemangat untuk mulai menyediakan sumber daya ini kepada sukarelawan di masyarakat.
“Para sukarelawan dalam uji coba ini adalah pahlawan,” kata Mullane. “Data yang berasal dari studi ini akan menginformasikan layanan kesehatan selamanya. Pendaftaran dalam uji coba fase 3 sangat penting karena studi ini jauh lebih besar daripada uji coba fase 1 dan 2 dan akan memberi kita lebih banyak informasi mengenai keefektifan vaksin. Kami sangat senang dapat bekerja dengan komunitas kami untuk membantu memastikan bahwa orang-orang dari semua ras memiliki kesempatan yang sama untuk berpartisipasi dalam uji coba ini dan terwakili dengan baik.”
Para peneliti mengantisipasi UChicago Medicine menjadi tempat uji coba vaksin COVID-19 tambahan dalam beberapa bulan ke depan. Sementara itu, uji klinis lain yang sedang berlangsung di UChicago Medicine sedang memeriksa efektivitas pengobatan untuk COVID-19, termasuk plasma konvalesen , antibodi penetralisir, dan remdesivir , obat antivirus spektrum luas.
Rumah Sakit Chicago Dapatkan Grade A untuk Keselamatan Pasien
hospitalmicrobiome – Enam rumah sakit Chicago menerima “A” untuk keselamatan pasien dalam evaluasi yang dirilis Senin oleh The Leapfrog Group , sebuah kelompok pengawas nirlaba nasional.
Rumah Sakit Chicago Dapatkan Grade A untuk Keselamatan Pasien – Dilakukan dua kali setahun, The Leapfrog Group memberikan nilai tertinggi untuk rumah sakit berikut dalam evaluasi musim gugur 2016:
Rumah Sakit Chicago Dapatkan Grade A untuk Keselamatan Pasien
Advokat Illinois Masonic Medical Center
Pusat Medis Kebangkitan Kehadiran
Pusat Medis Kehadiran Saints Mary dan Elizabeth
Pusat Medis Universitas Rush
Rumah Sakit Saint Anthony
Pusat Medis Universitas Chicago
Dimulai pada tahun 2012, Tingkat Keselamatan Rumah Sakit Leapfrog menilai lebih dari 2.600 rumah sakit AS pada 30 tindakan keselamatan pasien yang berbeda, termasuk infeksi dan masalah dengan pembedahan, yang digunakan dalam program pengukuran dan pelaporan nasional. Rumah sakit diberi nilai huruf (dari “A,” “B,” “C,” “D,” atau “F”) berdasarkan langkah-langkah tersebut.
Advokat Illinois Masonic Medical Center, Rush University Medical Center, dan University of Chicago Medical Center telah memperoleh 10 nilai “A” berturut-turut—suatu perbedaan yang hanya diperoleh 72 rumah sakit di negara ini.
“Saya bangga dengan konsistensi dan dedikasi yang luar biasa dari semua orang yang merawat pasien kami di Rush selama lima tahun Leapfrog menilai rumah sakit,” kata Presiden dan COO Pusat Medis Universitas Rush Michael Dandorph dalam sebuah pernyataan.
“Hal terbaiknya adalah ini menunjukkan kepada pasien bahwa mereka dapat merasa yakin bahwa ketika mereka berada di Rush, mereka akan aman dari jenis komplikasi yang dapat dihindari yang dapat membuat pasien lebih buruk daripada lebih baik.”
Setiap tahun lebih dari 206.000 orang meninggal akibat kesalahan medis di rumah sakit AS, menjadikannya penyebab kematian ketiga, menurut The Leapfrog Group .
“Untuk pasien dan keluarga mereka, keselamatan rumah sakit bisa menjadi masalah hidup dan mati,” Sharon O’Keefe, presiden Pusat Medis Universitas Chicago mengatakan dalam siaran pers. “Kami bekerja dengan karyawan kami – semua orang mulai dari staf pendukung hingga dokter garis depan – untuk membangun dan mempertahankan budaya di mana keselamatan adalah yang terpenting, yang memastikan kami memberikan perawatan terbaik bagi pasien kami.”
Advokat Wakil Presiden Eksekutif Perawatan Kesehatan dan Kepala Petugas Medis Dr. Lee Sacks mengatakan rumah sakit itu “bangga diakui.”
“Keselamatan pasien adalah prioritas utama organisasi kami dan tertanam dalam budaya kami di setiap tingkat,” kata Sacks dalam siaran pers. “Dokter, perawat, dan rekan kami mengambil tanggung jawab ini dengan sangat serius dan tetap berkomitmen untuk memastikan hasil terbaik bagi pasien, yang pantas mendapatkan yang terbaik.”
Secara nasional, hanya 844 rumah sakit dari 2.633 yang mendapatkan nilai “A.” Dari 113 rumah sakit yang diperingkat di Illinois, 45 mendapatkan “A,” menempatkan negara bagian itu ke tempat No. 15 dalam keselamatan pasien secara nasional. Selain rumah sakit Advocate, Rush, dan University of Chicago, 11 rumah sakit Illinois lainnya telah mendapatkan 10 nilai “A” berturut-turut. Mereka:
Pusat Medis Rush Copley
Rumah Sakit HSHS St. Joseph, Breese
Pusat Medis OSF St. Joseph
Rumah Sakit Peringatan Elmhurst
Pusat Medis Suburban Barat
Pusat Medis OSF St. Mary
Rumah Sakit Morris
Advokat Rumah Sakit Umum Lutheran
Rumah Sakit DuPage Pusat Pengobatan Barat Laut
Advokat Rumah Sakit Samaria yang Baik
AMITA Health Hoffman Estates
Di seluruh negeri, 648 rumah sakit mendapatkan “B”; 954 mendapatkan “C”; 157 mendapatkan “D”; dan 20 mendapatkan “F.” Tidak ada rumah sakit Chicago yang mendapatkan nilai “F”, tetapi Rumah Sakit Loretto, Rumah Sakit dan Pusat Medis Mercy, Rumah Sakit Komunitas Roseland, dan Rumah Sakit Universitas Illinois masing-masing mendapatkan nilai “D” dari Grup Leapfrog.
“Dalam lanskap perawatan kesehatan yang berubah dengan cepat, pasien harus menyadari bahwa rumah sakit tidak semuanya kompeten dalam melindungi mereka dari cedera dan infeksi,” kata Presiden dan CEO Leapfrog Leah Binder dalam siaran pers.
“Kami percaya setiap orang memiliki hak untuk mengetahui rumah sakit mana yang paling aman dan mendorong anggota masyarakat untuk menyerukan rumah sakit setempat mereka untuk berubah, dan pada pejabat terpilih mereka untuk mendorong mereka bertindak.”
Baca Juga : MGC Mengambil Alih Perusahaan Riset Penelitian Medis Internasional
Ingin tahu aman rumah sakit Anda? Cari peringkat Leapfrog berdasarkan nama rumah sakit, kode pos atau kota dan negara bagian untuk informasi lebih lanjut. Agar rumah sakit menerima peringkat keselamatan, ia harus menyediakan data keamanan yang cukup untuk dianalisis oleh para ahli. Penilaian Leapfrog terhadap rumah sakit tidak termasuk rumah sakit VA, rumah sakit akses kritis, rumah sakit khusus atau pusat operasi rawat jalan.
MGC Mengambil Alih Perusahaan Riset Penelitian Medis Internasional
hospitalmicrobiome – MGC Pharmaceuticals yang terdaftar di ASX telah mengambil alih perusahaan penelitian klinis dan medis internasional MediCaNL yang sekarang akan melakukan semua uji klinis sebagai unit internal perusahaan.
MGC Mengambil Alih Perusahaan Riset Penelitian Medis Internasional – Akuisisi ini diharapkan menghasilkan penghematan biaya dan peningkatan efisiensi yang signifikan serta memperkuat keahlian internal dan peluang untuk memperluas hubungan regulasi. Tiga uji klinis yang direncanakan untuk tahun ini saja sekarang akan dilakukan secara internal melalui MediCaNL.
MGC Mengambil Alih Perusahaan Riset Penelitian Medis Internasional

MGC bercita-cita untuk mengembangkan dan memasok obat-obatan turunan phytocannabinoid yang terjangkau dan terstandarisasi untuk penggunaan global, dengan fokus pada dua kondisi medis yang tersebar luas pada epilepsi dan demensia. Produk lebih lanjut sedang dalam pengembangan sementara kolaborasi penelitian internasional sedang berlangsung termasuk untuk penggunaan phytocannabinoid dalam mengobati tumor otak.
Perusahaan sekarang telah mengambil langkah penting dalam mengurangi biaya dan mengurangi birokrasi ketat yang terlibat dalam melakukan uji klinis untuk penelitian dan penawaran produknya. Akuisisi MediCaNL tampaknya telah menempatkan MGC pada posisi efisiensi operasional yang lebih baik.
Berbasis di Israel, MediCaNL mengkhususkan diri dalam seluruh proses penelitian medis untuk ganja obat yang menawarkan layanan uji klinis dan pra-klinis. Perusahaan saat ini mengelola uji klinis di Israel, Eropa dan Australia, membimbing kliennya selama proses penelitian dari konsep hingga pengembangan sementara juga memberikan dukungan data penelitian.
CEO MediCaNL, Dr Nadya Lisodover telah berkolaborasi dengan MGC selama dua tahun terakhir mengarahkan uji klinis perusahaan dan memberikan saran peraturan sebagai konsultan Chief Research Officer. Dr Lisodover sekarang akan bekerja penuh waktu untuk MGC.
Tidak termasuk MGC, MediCaNL saat ini memiliki 11 klien dengan 40 proyek yang sedang berjalan dan pada tahun 2020 saja menghasilkan pendapatan sekitar A$1 juta dengan margin keuntungan 25 persen.
Setelah akuisisi selesai, MediCaNL akan menjadi unit bisnis internal MGC yang merancang, mengelola, dan menjalankan semua uji klinis sesuai dengan persyaratan peraturan internasional. Ini akan beroperasi dengan biaya untuk MGC, menghilangkan margin operasi ritel yang sebelumnya dikeluarkan untuk uji klinis yang dijalankan oleh penyedia pihak ketiga.
MGC berencana untuk melakukan banyak uji klinis tahun ini dan seterusnya dengan akuisisi yang tampaknya telah menempatkan perusahaan pada posisi yang kuat dalam upaya operasionalnya. Tahun ini saja, MGC memiliki tiga uji klinis terpisah untuk produk CannEpil, CogniCann, dan CimetrA.
Uji coba Fase IIb untuk CannEpil sebagai bentuk pengobatan yang aman dan efektif bagi anak-anak dan remaja dengan epilepsi refrakter telah dimulai di Rumah Sakit Schindler di Israel.
Di Universitas Notre Dame di Perth, uji coba Fase II untuk menilai manfaat perilaku CogniCann untuk pasien dengan demensia dan penyakit Alzheimer juga telah dimulai.
Sementara itu di Rambam Health Care Campus di Israel, uji coba Fase III untuk penggunaan CimetrA dalam pengobatan COVID-19 telah diberi lampu hijau peraturan.
Berdasarkan ketentuan akuisisi, yang tetap harus mendapat persetujuan pemegang saham, MediCaNL akan mengakuisisi saham di MGC sebesar A$6 juta, di mana 30 persen akan diterbitkan setelah penyelesaian transaksi dan 70 persen sisanya akan diterbitkan. dicicil selama 13 bulan.
Baca Juga : Paparan Mikroorganisme Lingkungan dan Asma Anak
Mengingat bahwa sedikit, jika ada topik di seluruh dunia yang lebih penting daripada perawatan kesehatan, peningkatan efisiensi dan manfaat pemotongan biaya dari akuisisi MediCaNL hanya dapat menjadi pertanda baik bagi rencana ambisius MGC untuk mengirimkan produk obatnya yang luas ke pasar global.
Paparan Mikroorganisme Lingkungan dan Asma Anak
hospitalmicrobiome – Anak-anak yang tumbuh di lingkungan yang memberikan mereka berbagai paparan mikroba, seperti pertanian tradisional, dilindungi dari asma dan atopi masa kanak-kanak. Dalam penelitian sebelumnya, penanda paparan mikroba berbanding terbalik dengan kondisi ini.
Paparan Mikroorganisme Lingkungan dan Asma Anak – Dalam dua studi cross-sectional, kami membandingkan anak-anak yang tinggal di peternakan dengan anak-anak dalam kelompok referensi sehubungan dengan prevalensi asma dan atopi dan keragaman paparan mikroba. Dalam satu penelitian PARSIFAL (Pencegahan Alergi Faktor Risiko untuk Sensitisasi pada Anak Terkait dengan Pertanian dan Gaya Hidup Antroposofis) sampel debu kasur disaring untuk DNA bakteri dengan menggunakan analisis polimorfisme konformasi untai tunggal (SSCP) untuk mendeteksi bakteri lingkungan yang tidak dapat diukur dengan teknik budaya. Dalam studi lain GABRIELA (Studi Multidisiplin untuk Mengidentifikasi Penyebab Genetik dan Lingkungan Asma di Komunitas Eropa [GABRIEL] Studi Lanjutan) sampel debu menetap dari kamar anak-anak dievaluasi untuk taksa bakteri dan jamur dengan menggunakan teknik kultur.
Paparan Mikroorganisme Lingkungan dan Asma Anak
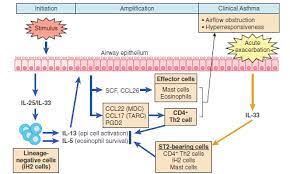
Dalam kedua penelitian, anak-anak yang tinggal di pertanian memiliki prevalensi asma dan atopi yang lebih rendah dan terpapar lebih banyak mikroorganisme lingkungan daripada anak-anak dalam kelompok referensi. Pada gilirannya, keragaman paparan mikroba berbanding terbalik dengan risiko asma (rasio odds untuk PARSIFAL, 0,62; interval kepercayaan 95% [CI], 0,44 hingga 0,89; rasio odds untuk GABRIELA, 0,86; 95% CI, 0,75 hingga 0,99) . Selain itu, adanya paparan tertentu yang lebih terbatas juga berbanding terbalik dengan risiko asma; ini termasuk paparan spesies di eurotium takson jamur (rasio odds yang disesuaikan, 0,37; 95% CI, 0,18 hingga 0,76) dan berbagai spesies bakteri, termasuk Listeria monocytogenes, spesies bacillus, spesies corynebacterium, dan lainnya (rasio odds yang disesuaikan, 0,57; 95% CI, 0,38 hingga 0,86). Anak-anak yang tinggal di pertanian terpapar mikroba yang lebih luas daripada anak-anak dalam kelompok referensi, dan paparan ini menjelaskan sebagian kecil dari hubungan terbalik antara asma dan tumbuh di pertanian. (Didanai oleh Deutsche Forschungsgemeinschaft dan Komisi Eropa.)
Paparan lingkungan terhadap mikroorganisme telah berulang kali ditemukan berbanding terbalik dengan manifestasi penyakit atopik seperti asma dan demam. Pengamatan ini dilakukan dalam berbagai konteks, termasuk studi yang dilakukan di Republik Karelia (Rusia) dan Karelia Utara (Finlandia), di mana dua populasi di wilayah yang berdekatan secara geografis hidup dalam kondisi lingkungan yang berbeda. Pada populasi dengan pajanan bakteri yang lebih tinggi, prevalensi asma dan atopi secara substansial lebih rendah. Contoh lain yang mendukung gagasan ini adalah prevalensi asma dan atopi yang lebih rendah di antara anak-anak yang dibesarkan di pertanian. Banyak penelitian menggunakan produk mikroba, seperti endotoksin atau asam muramat,sebagai penanda sederhana paparan mikroba telah menguatkan pengamatan ini.
Dalam studi epidemiologi saat ini, kami mengkarakterisasi paparan mikroba terkait pertanian di luar penanda sederhana yang disebutkan di atas. Kami menggunakan data dari dua studi observasional skala besar terhadap anak-anak sekolah yang tinggal di sebagian besar daerah pedesaan Eropa Tengah: populasi Jerman dari studi PARSIFAL (Pencegahan Alergi Faktor Risiko untuk Sensitisasi Terkait Pertanian dan Gaya Hidup Antroposofi) dan populasi Bavaria di GABRIELA (Studi Multidisiplin untuk Mengidentifikasi Penyebab Genetik dan Lingkungan Asma dalam Studi Lanjutan Komunitas Eropa [GABRIEL]). Kami menilai prevalensi asma dan atopi di antara anak-anak yang tinggal di pertanian dan di antara anak-anak lain yang tinggal di daerah yang sama (kelompok referensi), mengukur keragaman paparan mikroba pada kedua kelompok, dan terkait keragaman paparan asma dan atopi.
Karakteristik kedua populasi penelitian, sampel yang dianalisis, dan jenis analisis yang dilakukan dirangkum. Studi PARSIFAL adalah survei cross-sectional termasuk anak-anak petani, anak-anak menghadiri sekolah Rudolf Steiner (yaitu, sekolah antroposofis), dan kelompok referensi masing-masing. 6Di Bavaria, Jerman, 6963 anak usia sekolah (6 sampai 13 tahun) dari daerah pedesaan atau pinggiran kota berpartisipasi. Dalam subsampel anak-anak yang dipilih secara acak, analisis sampel darah dan debu dilakukan. Untuk sampel tersebut, semua anak yang disetujui oleh orang tua atau walinya memenuhi syarat (55% anak yang tinggal di pertanian dan 48% anak yang tidak tinggal di pertanian). Di antara 801 anak yang sampel debunya dikumpulkan, sampel untuk 489 anak mengandung jumlah debu yang cukup untuk analisis SSCP.
Baca Juga : Perubahan Ekologi Mikrobioma Saluran Pernapasan dan Pneumonia Nosokomial
GABRIELA adalah studi cross-sectional yang dilakukan di sekolah dasar di lima daerah pedesaan di selatan Jerman, Swiss, Austria, dan Polandia; karena perbedaan dalam desain penelitian, data Polandia tidak dilaporkan di sini. Dari 34.491 anak antara usia 6 dan 12 tahun yang direkrut, sampel acak berlapis dari 9668 anak dipilih. Tiga strata dalam sampel ditentukan oleh tingkat paparan pertanian yang berbeda, dari tidak terpapar hingga paparan menengah hingga tinggal di pertanian. Stratified, random subsampling kemudian dilakukan di Bavaria, Jerman, dengan sampling lingkungan dilakukan pada 444 anak dan pengukuran fungsi paru dilakukan pada 895 anak.
Informed consent tertulis diperoleh dari orang tua atau wali dari semua anak yang berpartisipasi. Untuk kedua studi tersebut, komite etik dari universitas yang berpartisipasi dan otoritas perlindungan data regional menyetujui kedua studi tersebut.Dalam kedua studi, kuesioner digunakan untuk menilai gejala dan diagnosis pernapasan dan alergi, paparan terkait pertanian pada berbagai usia, dan pembaur potensial. Anak-anak yang tinggal penuh waktu di pertanian yang dikelola keluarga diklasifikasikan sebagai anggota kelompok tani, sedangkan semua anak lainnya diklasifikasikan sebagai anggota kelompok referensi. Asma didefinisikan sebagai diagnosis asma yang ditegakkan oleh dokter setidaknya satu kali atau diagnosis bronkitis mengi yang ditegakkan lebih dari satu kali. Atopi didefinisikan oleh adanya antibodi IgE spesifik terhadap Dermatophagoides pteronyssinus(tungau debu), antigen kucing, campuran pohon (dalam studi PARSIFAL), atau birch (dalam GABRIELA) minimal 0,7 kU per liter atau reaksi positif terhadap campuran rumput minimal 0,35 kU per liter. Antibodi IgE dideteksi melalui sistem Pharmacia CAP dan UNICAP 1000, Phadia AB, Uppsala, Swedia.
Dalam studi PARSIFAL, debu dari kasur anak-anak dikumpulkan seperti yang dijelaskan sebelumnya.Sampel debu dilarutkan dalam saline buffer fosfat, dan ekstraksi DNA dan analisis SSCP dilakukan seperti yang dilaporkan sebelumnya. Sebuah fragmen dari daerah variabel 4 dan 5 dari DNA ribosom 16S diamplifikasi dan dianalisis pada gel SSCP. Analisis profil SSCP dilakukan dengan perangkat lunak GelCompar II, versi 4.6 (Matematika Terapan). Gel SSCP dinormalisasi dengan menggunakan standar tambahan yang ada dalam dua atau tiga lintasan pada setiap gel. Pita yang menarik dikeluarkan dari setidaknya tiga trek individu, diperkuat, dan diurutkan. Urutan DNA dianalisis untuk kesamaan setidaknya 98% dengan penggunaan Proyek Basis Data Ribosom II untuk analisis filogenetik.
Di GABRIELA, sampel debu di udara dikumpulkan dengan menggunakan pengumpul debu elektrostatik. Kolektor ini adalah tempat sampel plastik yang dilengkapi dengan kain elektrostatik yang berpotensi untuk menangkap debu dari udara. Para kolektor ditempatkan di kamar tidur anak-anak oleh pekerja lapangan dan dibiarkan di sana selama 14 hari. Kain dicuci dengan polisorbat 80, dan pengenceran larutan pencuci secara sistematis dilapisi pada lima media pertumbuhan yang berbeda. Setelah inkubasi selama 7 hari, koloni dihitung dan diidentifikasi berdasarkan penilaian kasar dan mikroskopis. Koloni bakteri juga diperlakukan dengan pewarnaan Gram. Hasil bakteri dan jamur dinyatakan sebagai unit pembentuk koloni per pengumpul debu.
Dalam studi PARSIFAL, paparan bakteri dimodelkan dengan menggunakan variabel dikotomis, dengan titik potong 5 unit kepadatan yang sesuai dengan ambang batas deteksi visual pada gel. Untuk analisis faktor, variabel kontinu yang mewakili nilai densitas gel untuk 76 pita digunakan. Karena distribusi miring dan beberapa nilai nol, nilai kerapatan pita, mulai dari 0 hingga 160, ditambah 1 dan ditransformasi log.
Dalam GABRIELA, paparan mikroba diwakili oleh variabel dikotomis untuk enam taksa bakteri dan sembilan taksa jamur (terdeteksi vs tidak terdeteksi). Taksa tambahan ditemukan pada kurang dari 10% dari semua anak dan dikeluarkan dari analisis lebih lanjut. Karena desain pengambilan sampel bertingkat di GABRIELA, metode statistik tertimbang diterapkan dengan menggunakan metode deret Taylor untuk estimasi varians.
Untuk penilaian keragaman mikroba, skor dihasilkan dengan menjumlahkan semua pita yang dapat dideteksi (PARSIFAL) dan semua taksa jamur (GABRIELA). Pendekatan ini tidak layak untuk taksa bakteri di GABRIELA, bagaimanapun, karena mereka diklasifikasikan terutama berdasarkan kriteria kasar seperti pewarnaan Gram. Probabilitas asma atau tinggal di pertanian dihitung sebagai nilai prediksi dari regresi logistik untuk asma atau tinggal di pertanian, dengan nilai keragaman masing-masing sebagai variabel independen.
Dalam studi PARSIFAL, reduksi data untuk 76 variabel densitas pita kontinu dicapai dengan melakukan analisis faktor dengan rotasi varimax. Faktor dengan nilai Eigen 1,5 atau lebih diekstraksi. Regresi logistik untuk asma dan atopi dilakukan untuk semua faktor atau taksa yang diekstraksi, dengan penyesuaian untuk kelompok studi (yaitu, tinggal atau tidak tinggal di pertanian). Nilai P, pada tingkat alfa efektif 0,05, dikoreksi untuk beberapa perbandingan dengan menerapkan metode Bonferroni (yaitu, tingkat alfa 0,05-10 untuk 10 faktor dalam studi PARSIFAL dan tingkat alfa 0,05-15 untuk 15 faktor). taksa di GABRIELA). Akhirnya, model regresi untuk asma dan atopi saling disesuaikan untuk eksposur atau faktor spesifik dan skor keragaman.
Perubahan Ekologi Mikrobioma Saluran Pernapasan dan Pneumonia Nosokomial
Pneumonia nosokomial merupakan salah satu infeksi yang paling sering terjadi pada pasien kritis.
hospitalmicrobiome – Hal ini terutama terkait dengan ventilasi mekanis yang menyebabkan penyakit parah, kematian yang tinggi, dan rawat inap yang berkepanjangan. Risiko kematian telah meningkat dari waktu ke waktu karena meningkatnya infeksi bakteri multidrug-resistant (MDR), yang merupakan ancaman kesehatan masyarakat global. Penelitian microbiome saluran pernapasan (RTM) sedang berkembang, dan penelitian terbaru menunjukkan bahwa RTM yang sehat secara positif merangsang sistem kekebalan tubuh dan, seperti mikrobioma usus, dapat melindungi terhadap infeksi patogen melalui resistensi kolonisasi (CR).
Perubahan Ekologi Mikrobioma Saluran Pernapasan dan Pneumonia Nosokomial – Kondisi fisiologis pasien kritis dan intervensi seperti pemberian antibiotik dan ventilasi mekanis secara dramatis mengubah RTM, menyebabkan disbiosis. Disbiosis RTM pasien ICU mendukung kolonisasi oleh patogen oportunistik dan resisten yang dapat menjadi bagian dari mikrobiota atau diperoleh dari lingkungan rumah sakit (biotik atau buatan). Meskipun bukti terbaru menunjukkan pentingnya RTM pada infeksi nosokomial, sebagian besar interaksi host-RTM tetap tidak diketahui. Dalam konteks ini, kami menyajikan perspektif kami mengenai penelitian di RTM yang mengubah ekologi di lingkungan klinis, terutama sebagai risiko untuk mendapatkan pneumonia nosokomial. Kami juga merefleksikan kesenjangan di lapangan dan menyarankan arah penelitian di masa depan. Selain itu, intervensi berbasis mikrobioma yang diharapkan bersama dengan alat untuk mempelajari RTM yang menyoroti pendekatan “omics” juga dibahas.
Perubahan Ekologi Mikrobioma Saluran Pernapasan dan Pneumonia Nosokomial
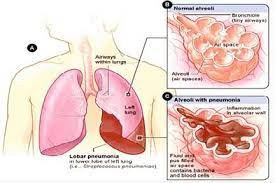
Saluran pernapasan adalah sistem organ yang berjalan dari lubang hidung ke alveoli paru-paru. Ini dibagi menjadi saluran pernapasan supratoraks (atas) (URT) dan saluran pernapasan intratoraks (bawah) (LRT) dengan permukaan sekitar 100 meter persegi . Selama bertahun-tahun, beberapa penelitian telah mengungkapkan keberadaan ekosistem mikroba residen yang menghuni permukaan saluran napas: mikrobioma saluran pernapasan (RTM), sangat padat di URT. Sebagai mikrobioma gastrointestinal (GIM), RTM merupakan ekosistem berkelanjutan dengan gradien longitudinal dan transversal keragaman mikroba dari rongga hidung dan mulut ke alveoli . Namun, RTM dan GIM berbeda dalam biomassa, keanekaragaman dan komposisi taksonomi.
Pada individu yang sehat, kompleksitas dan biomassa GIM meningkat dari lambung ke usus besar, mencapai 10 10 -10 12 CFUs/mL . Pada RTM, orofaring memiliki densitas bakteri yang tinggi (10 7 -10 8 CFU/ml), namun saat berpindah dari mulut ke paru-paru terjadi penurunan progresif, mencapai 10 4 -10 5 sel bakteri per mL alveolus. cairan intraluminal. Komposisi RTM dipengaruhi oleh kondisi pertumbuhan mikrobiologi lokal yang ditentukan oleh ketersediaan nutrisi, mikro-geografi, dan kondisi fisikokimia seperti eskalator mukosiliar, tekanan oksigen, aliran darah, pH, suhu, interaksi sistem kekebalan manusia, dan faktor lingkungan . Sumber utama mikroorganisme RTM adalah orofaring, yang akhirnya bermigrasi ke LRT melalui mikroaspirasi dan dispersi mukosa .
Model ekologi RTM saat ini dikenal sebagai “model pulau paru-paru yang diadaptasi” , dan menyerupai proses biogeografi, yang diturunkan dari model keseimbangan yang diusulkan oleh MacArthur dan Wilson (1963) dari biogeografi pulau . “Model yang disesuaikan” menunjukkan bahwa kekayaan mikroba dalam RTM didasarkan pada keseimbangan imigrasi (ekstensi mukosa, aspirasi mikro) dan eliminasi (pembersihan silia, batuk, mekanisme kekebalan antimikroba) spesies ke paru-paru dari URT. Pada dasarnya, struktur RTM tergantung pada laju migrasi stokastik, pertumbuhan, kepunahan, dan penyebaran epidemi anggota komunitas mikroba, proses yang dipengaruhi oleh faktor anatomi, fisiologis, dan klinis . Model ini akan membantu menjelaskan gradien keragaman mikroba, biomassa, dan penurunan kompleksitas dari rongga mulut ke paru-paru. Dickson dan rekan menyatakan bahwa, dalam kesehatan, mikrobioma paru-paru lebih dipengaruhi oleh imigrasi dan eliminasi mikroba daripada oleh kondisi pertumbuhan lokal. Namun, kondisi pertumbuhan lokal lebih kritis selama penyakit klinis lanjut. Model ekologi berbasis mikrobioma ini memberikan kerangka teoretis untuk infeksi patogen, lebih akurat daripada pandangan tradisional tentang pneumonia berdasarkan pertumbuhan cepat penyerang ke paru-paru steril.
Komposisi bakteri RTM yang sehat terutama terdiri dari Firmicutes, Bacteroidetes, dan Proteobacteria, yang merupakan tiga dari empat filum utama di semua mikrobioma spesifik lokasi manusia. Genera yang paling melimpah adalah Streptococcus, Prevotella , atau Veillonella , yang juga mendominasi dalam mikrobioma oral. Hanya beberapa penelitian yang mengkarakterisasi anggota RTM lainnya sebagai jamur, archaea, atau virus. Dengan kemungkinan pengecualian Saccharomycetes (sebagai genus Candida) di orofaring, sulit untuk memastikan apakah pada tingkat yang lebih rendah (sub-trakea) ada “mikobioma pernapasan” yang normal, jika jamur yang ditemukan di RTM sesuai dengan jamur lingkungan yang dihirup, atau jika sebagian dari mereka lebih sedikit.
rentan terhadap pembersihan fisiologis. Mycobiome pernapasan yang sehat diperkaya dengan jamur lingkungan dari filum Ascomycota dan Basidiomycota, yang paling umum juga di GIT. Banyak jamur sesuai dengan Eremothecium, Systenostrema, genus Cladosporium, dan keluarga Davidiellaceae yang, bersama dengan Saccharomycetes, juga merupakan taksa yang paling umum di GIT. Virome LRT sebagian besar masih belum dijelajahi, terutama pada orang sehat. Meskipun demikian, mirip dengan virom usus, virus eukariotik dan banyak bakteriofag telah dijelaskan dalam penelitian yang berbeda. Beberapa penelitian menunjukkan fungsi virom pernapasan dalam priming dan modulasi respon imun inang, serta kontrol spesies mikroba lain di dalam paru-paru.
Faktor-faktor yang membentuk keragaman virom tetap tidak diketahui, meskipun komposisinya di saluran pernapasan tampaknya ditentukan oleh kesehatan inang dan keberadaan populasi bakteri tertentu di bronkus, seperti yang telah disarankan pada cystic fibrosis . Sebuah studi metagenomik dari virome setelah transplantasi paru-paru berdasarkan sampel allograft bronchoalveolar lavage (BAL) menunjukkan bahwa saluran pernapasan penerima transplantasi paru-paru diperkaya dalam populasi kompleks anellovirus. Viral load juga telah berkorelasi dengan dysbiosis bakteri yang mempengaruhi hasil transplantasi dan menunjukkan bahwa interaksi virus-bakteri sangat penting untuk keseimbangan sistem mikrobioma-imun dan, dengan demikian, untuk fisiologinya.
Baca Juga : Agenda Penelitian untuk Mikrobiologi Dalam Ruangan, Kesehatan Manusia, dan Bangunan
Selain itu, kelimpahan bakteriofag yang tinggi di RTM layak untuk penelitian mendalam untuk menentukan apakah mereka memainkan peran yang sama seperti yang diamati di GIM, yaitu, mengendalikan homeostasis mikroba (mekar, komposisi mikroba, keragaman, metabolisme, dan memfasilitasi transfer gen horizontal ( HGT).Arkaea metanogenik telah terdeteksi di mikrobioma hidung, GIT, kulit, dan paru-paru, dan filum Woesearchaeota tampaknya berasosiasi dengan paru-paru. Namun, selain beberapa studi deskriptif, fungsi fraksi non-bakteri dari RTM layak untuk dianalisis lebih lanjut.
Ekologi RTM adalah bidang penelitian yang muncul yang mendapatkan perhatian karena beberapa penelitian menunjukkan peran menguntungkan dari penghuni mikroba dalam stimulasi sistem kekebalan dan perlindungan terhadap patogen (resistensi kolonisasi, CR), seperti yang telah didokumentasikan secara luas untuk mikrobioma usus. Homeostasis mikrobioma dapat terganggu sementara, misalnya, oleh penggunaan antibiotik, penggunaan peralatan medis (intubasi, ventilator), kejadian abnormal sementara (aspirasi), atau penyakit tertentu (penyakit virus dapat mengurangi efektivitas eskalator pembersihan bronkus) yang memungkinkan beberapa patogen untuk tumbuh terlalu cepat dan meningkatkan kolonisasi dan, pada akhirnya menyebabkan infeksi di LRT.
Sebagian besar penelitian yang terkait dengan RTM fokus pada penyakit pernapasan kronis tertentu seperti: B. Populasi mikroba yang mengkolonisasi paru-paru dengan cystic fibrosis. Pada penyakit ini, hiperviskositas saluran napas mendorong pertumbuhan multibakteri dan disbiosis di sepanjang saluran udara. Bakteri yang paling sering dikaitkan dengan kolonisasi kronis cystic fibrosis adalah Pseudomonas aeruginosa, Staphylococcus aureus, Stenotrophomonas maltophilia, Burkholderia, dan Pandoraea, yang sering berkolonisasi. Namun, ada juga mikroorganisme yang berhubungan dengan rongga mulut seperti actinomycetes, fusobacteria, gemella, granuricatella, neisseria, porphyromonas, prevotella, Russia, streptococcus, hemophilus, dan veillonella. Menariknya, pada pasien dengan cystic fibrosis, bakteri pemangsa RTMLRT seperti Bdellovibrio dan Bampirovibrio, serta parasit dari bakteri Parcubacteria phylumr TMS, ditemukan dalam memerangi populasi bakteri patogen.
Di sini, kami menyajikan perspektif kami mengenai penelitian dalam ekologi RTM yang berubah di lingkungan klinis, meningkatkan kemungkinan untuk memperoleh pneumonia nosokomial di area rumah sakit berisiko tinggi sebagai ICU, dan mendiskusikan kemajuan terbaru pada topik tersebut. Kami juga membahas kesenjangan di lapangan, masa depan intervensi berbasis mikrobioma untuk mencegah dan mengobati pneumonia nosokomial, dan kontribusi pendekatan “omics” untuk memahami peran dinamika RTM dalam timbulnya infeksi pernapasan.
Ekologi Mikrobioma Pernapasan pada Pneumonia Nosokomial
Infeksi LRT akut, pneumonia atau eksaserbasi bronkitis kronis, adalah penyebab utama mortalitas dan morbiditas di seluruh dunia. Pada orang tua, perkembangan pneumonia terjadi cepat, dengan prognosis buruk, terutama terkait dengan rawat inap, dan angka kematian yang tinggi sering di ICU. Pneumonia nosokomial, infeksi alveolus paru yang sebagian besar disebabkan oleh bakteri, tetapi juga virus, atau jamur terdiri dari pneumonia yang didapat di rumah sakit dan terkait ventilator dan merupakan masalah kesehatan masyarakat yang signifikan karena sering disebabkan oleh patogen yang resistan terhadap banyak obat (MDR) yang didapat di dalam paru-paru. lingkungan rumah sakit.
Pneumonia terkait ventilator merupakan penyebab pertama infeksi nosokomial pada pasien dengan ventilasi mekanik dan kedua tersering di unit perawatan intensif (ICU), dengan infeksi jangka panjang yang sering disebabkan oleh bakteri MDR. Skenario ini telah memburuk selama pandemi COVID-19 karena peningkatan dramatis dalam infeksi sekunder SARS-CoV-2 dan penggunaan antibiotik yang berlebihan, yang menyebabkan peningkatan yang luar biasa dari infeksi MDR dan transmisi gen resistensi antibiotik (ARGs). Kontribusi mikrobioma terhadap respons imun bawaan dan adaptif menunjukkan bahwa mikrobioma yang sehat dapat menjadi faktor yang berkontribusi terhadap rasio kematian kasus yang lebih rendah dari COVID-19. Di sisi lain, disbiosis mikrobioma dapat dikaitkan dengan respons imun yang buruk dan hasil penyakit yang lebih buruk. Bidang ini baru dan studi yang tersedia mengenai mikrobioma COVID-19 telah melaporkan hasil yang kontradiktif.
Salah satu faktor yang menyebabkan kontradiksi tampaknya menjadi perancu seperti ventilasi mekanis pada pasien ICU, mengubah struktur komunitas RTM, termasuk banyaknya taksa oral yang sebelumnya terkait dengan COVID-19. Studi pengambilan sampel paru-paru yang terinfeksi secara langsung melalui bronkoskopi telah terbukti paling akurat sejauh ini untuk mengidentifikasi tanda tangan mikrobiologis dan imunologis alveolar yang terkait dengan infeksi SARS-CoV-2. Sebuah penelitian berdasarkan 142 pasien yang menjalani bronkoskopi menunjukkan bahwa hasil klinis sebagian dapat dijelaskan oleh kelimpahan virus alveolar, dan kolonisasi oleh bakteri turunan mikrobioma URT ( Mycoplasma salivarium ), dan respons imun adaptif yang buruk.
Model ekologi pneumonia mengusulkan bahwa keseimbangan RTM dipindahkan ke keadaan disbiosis yang ditandai dengan keragaman mikroba yang rendah, beban mikroba yang tinggi, dan respons inflamasi inang. Apakah disbiosis adalah penyebab atau efek dari penyakit pneumonia masih belum jelas. Faktanya, peran dan dinamika mikrobioma RTM pada pasien kritis hampir tidak diselidiki, dan oleh karena itu intervensi yang diarahkan mikrobioma belum dimasukkan dalam pedoman klinis. Tentu saja, gangguan RTM dapat dipengaruhi oleh keadaan fisiologis yang mengubah ekologi lokal, termasuk: (1) peradangan, perubahan profil metabolit, dan mekanisme pertahanan lokal yang melemah oleh infeksi (yaitu, virus), mendukung migrasi dan pertumbuhan stokastik bakteri ; (2) komposisi kimia abnormal dari bronkus, seperti pada cystic fibrosis ; (3) kelainan anatomi dan kondisi lain yang menyebabkan obstruksi, seperti pada bronkiektasis, cystic fibrosis, penyakit paru obstruktif kronik, edema paru (yang dapat menjadi sekunder untuk sepsis), atau kanker paru-paru; (4) kondisi berbahaya eksternal, seperti paparan jangka panjang terhadap dingin, yang menyebabkan vasokonstriksi mukosa pada mukosa saluran pernapasan dan penekanan respons imun, atau pemicu alergi untuk asma; (5) peningkatan migrasi bakteri (yaitu, aspirasi menyeluruh cairan lambung, perubahan mikrobioma oral, intubasi, ketidaksadaran, posisi terlentang), dan penurunan proses eliminasi (tidak sadar, intubasi, obat penenang, kepala terangkat, gangguan pembersihan mukosiliar) ; (6) penyakit yang mendasari dan intervensi medis (yaitu, imunosupresi terapeutik, intubasi, ventilasi mekanis, atau terapi antibiotik jangka panjang) yang mendukung kolonisasi patogen oportunistik.
Pneumonia nosokomial dapat bersifat endogen, yang disebabkan oleh patogen oportunistik seperti Streptococcus pneumoniae atau Haemophilus influenzae , yang merupakan bagian dari RTM manusia yang sehat. Pneumonia ini umumnya muncul segera setelah masuk. Namun, kasus perkembangan pneumonia yang terlambat sering melibatkan patogen MDR yang didapat di rumah sakit, termasuk P. aeruginosa , Enterobacteriaceae yang memproduksi extended spectrum beta lactamases (ESBL), dan/atau carbapenemases, dan Methicillin-resistant Staphylococcus aureus (MRSA), yang sering diseleksi dan tersebar di lingkungan ICU. Pandangan patogen-sentris penyakit menular baru-baru ini bergerak ke arah perspektif ekologis berdasarkan interaksi host-patogen-mikrobioma-lingkungan. Dalam konteks ini, pneumonia nosokomial mewakili skenario kompleks di mana beberapa faktor mungkin berperan dalam timbulnya dan hasil infeksi.
Agenda Penelitian untuk Mikrobiologi Dalam Ruangan, Kesehatan Manusia, dan Bangunan
Agenda Penelitian untuk Mikrobiologi Dalam Ruangan, Kesehatan Manusia, dan Bangunan – Ada hubungan yang ditunjukkan antara paparan mikroorganisme menular yang ada di lingkungan buatan dan kesehatan manusia. Dalam sejumlah kasus, mekanisme penularan dipahami dengan baik, tetapi lebih banyak yang dapat dipelajari tentang bagaimana desain lingkungan yang dibangun mempengaruhi proliferasi atau transmisi mikroorganisme menular tersebut.
Agenda Penelitian untuk Mikrobiologi Dalam Ruangan, Kesehatan Manusia, dan Bangunan

Baca Juga : Perlindungan Terhadap Orang yang Hidup Dengan Human Immunodeficiency Virus
hospitalmicrobiome – Ada bukti hubungan antara paparan mikroorganisme dalam ruangan dan perkembangan gejala pernapasan dan alergi, terutama yang timbul dari paparan mikroorganisme yang berkembang dalam pengaturan dalam ruangan yang lembab. Bukti awal menunjukkan bahwa paparan mikroba tertentu, termasuk paparan awal kehidupan terhadap beragam mikroorganisme yang terkait dengan hewan, mungkin memiliki efek kesehatan yang menguntungkan, seperti perlindungan dari alergi dan gejala pernapasan.
Sejumlah dampak kesehatan potensial tambahan (menguntungkan atau merugikan) yang terkait dengan paparan mikroorganisme dalam ruangan sedang dieksplorasi. Dampak pada hasil nonrespirasi (misalnya, neurologis) kurang dipahami dengan baik. Penyelidikan lebih lanjut diperlukan untuk memahami paparan mana yang mungkin menguntungkan atau merugikan dan dengan mekanisme apa.
Studi tambahan akan diperlukan untuk mengklarifikasi hubungan sebab akibat antara paparan mikroba di lingkungan binaan dan dampak kesehatan. Ini harus mencakup studi longitudinal lebih lanjut pada manusia dengan hewan pelengkap dan studi in vitro untuk menilai bagaimana tahap kehidupan, rute paparan, paparan bersama, dosis, dan sensitivitas genetik mempengaruhi hubungan paparan mikroba dalam ruangan individu dengan hasil kesehatan.
Bagaimana mikrobioma dari lingkungan dalam ruangan yang berbeda di mana manusia menghabiskan waktu untuk bekerja, hidup, belajar, dan bermain berdampak pada kesehatan dan kesejahteraan manusia? Kondisi bangunan apa yang mendukung komunitas mikroba yang menguntungkan atau merugikan kesehatan dan kesejahteraan manusia? Jika sebagian besar mikroorganisme tidak menginfeksi manusia, apakah mikroorganisme yang tumbuh subur di lingkungan dalam ruangan memengaruhi kesehatan manusia baik atau buruk, dan jika ya, melalui mekanisme apa? Pertanyaan-pertanyaan ini adalah di antara mereka yang memotivasi studi mikrobioma lingkungan binaan. Bab ini dimulai dengan meletakkan dasar untuk memahami bagaimana mikroorganisme yang ditemukan di bangunan dapat mempengaruhi kesehatan.
Bab ini kemudian membahas, pada gilirannya, penularan infeksi di lingkungan dalam ruangan, hasil kesehatan tidak menular yang terkait dengan mikroorganisme dalam ruangan, dan manfaat potensial dari paparan mikroba.Bagaimana karakteristik bangunan dan penghuni membentuk mikrobioma dalam ruangan, alat yang dapat digunakan dalam penelitian tentang mikrobioma lingkungan binaan, dan intervensi potensial yang dapat mengubah mikrobioma ini.
Beberapa pertimbangan mendukung masuk akal pengaruh membangun mikrobioma pada kesehatan manusia. Pertama, di daerah maju di dunia, lingkungan dalam ruangan adalah ekosistem utama yang dihuni oleh manusia. Kedua, lingkungan yang didiami orang dapat mempengaruhi mikrobioma manusia, yang pada gilirannya dapat berdampak pada kesehatan manusia. Misalnya, mikroorganisme yang ada di lingkungan dapat berkembang biak di ekosistem khusus inang manusia—seperti di saluran udara, usus, dan di kulit. Ketiga, beragam komponen dan karakteristik mikroba diketahui berdampak kesehatan manusia. Akhirnya, sejumlah sumber mikroorganisme dalam lingkungan dalam ruangan berdampak pada kesehatan manusia.
Di daerah maju di dunia, manusia dilahirkan dan menghabiskan sebagian besar hidup mereka di dalam ruangan, yang dapat membatasi keragaman mikroorganisme yang mereka terpajan. Selubung bangunan (pondasi, dinding, jendela, dan atap) memisahkan lingkungan dalam dan luar ruangan, sehingga mengurangi paparan mikroorganisme yang berkembang biak di luar ruangan dan berpotensi meningkatkan paparan organisme yang berkembang di dalam ruangan.
Keragaman mikrobioma dari lingkungan binaan di mana manusia hidup dapat mempengaruhi mikrobioma tubuh mereka. Penelitian telah menunjukkan bahwa manusia yang menghabiskan banyak waktu di luar ruangan atau tinggal di tempat tinggal dengan desain selubung bangunan yang lebih terbuka yang menghasilkan pertukaran udara tanpa filter atau filter minimal dengan tingkat tinggi dengan luar ruangan memiliki mikrobioma yang lebih beragam dibandingkan dengan mereka yang tinggal di tempat tinggal dengan desain yang kurang terbuka.
Sejauh mana mikrobioma dalam ruangan berkontribusi pada keragaman ini atau kekurangannya tidak dipahami dengan baik. Juga telah disarankan bahwa paparan terhadap keanekaragaman mikroba (terutama bakteri) yang berkurang mungkin kurang merupakan fungsi kandungan mikroba bangunan daripada efek samping dari makanan manusia modern, yang kurang beragam dibandingkan nenek moyang kita: itu sedikit berbeda dengan musim; mungkin terpengaruh oleh penggunaan antibiotik; dan dapat memilih taksa mikroba manusia dalam jumlah terbatas, terutama di usus.
Keragaman ini dapat bermanfaat bagi kesehatan manusia karena mikrobioma yang terpapar pada manusia mungkin penting untuk perkembangan kekebalan dan pemrosesan nutrisi dalam usus, yang mungkin tidak berfungsi dengan baik ketika komunitas mikroba usus berubah. Orang-orang di masyarakat yang kurang beruntung secara ekonomi dan kurang berkembang yang menghabiskan lebih banyak waktu di luar ruangan dapat memiliki risiko penyakit menular yang lebih tinggi dan kematian bayi yang lebih tinggi.
Namun, ini mungkin lebih disebabkan oleh kesehatan mereka ketika terpapar agen infeksi daripada keragaman mikroorganisme yang mereka terpajan; seperti dicatat, beberapa bukti menunjukkan efek sistem kekebalan yang menguntungkan dari paparan mikroba yang beragam (lihat bagian tentang “Efek Menguntungkan dari Mikroba”). Dengan demikian, relatif kurangnya keragaman mikroba mungkin memiliki efek positif atau merugikan pada respon fisiologis dan kekebalan manusia dan kesehatan dan pada gilirannya dapat mempengaruhi risiko gejala dan penyakit noninfeksi kronis. Dengan memisahkan diri dari alam bebas, manusia mungkin telah mengikis keanekaragaman mikrobioma mereka sendiri, serta lingkungan mereka.
Semakin banyak bukti menunjukkan bahwa mikrobioma manusia dipengaruhi oleh lingkungan dan merupakan bagian integral dari perkembangan manusia. Salah satu pengaruh yang paling banyak dipelajari adalah transmisi mikroorganisme menular tertentu. Misalnya, fomites adalah permukaan atau objek di mana mikroorganisme dapat menyimpan dan memungkinkan transmisi ke inang. Fomites didokumentasikan dengan baik dalam penyebaran penyakit menular, dan ada penelitian yang terkait dengan paparan patogen dalam ruangan pada manusia.
Pengaruh lain yang diketahui dari mikrobioma lingkungan pada mikrobioma manusia adalah proses kelahiran. Mikrobioma setiap individu diperoleh baik di dalam rahim maupun dari lingkungan saat lahir. Bayi yang dilahirkan pervaginam dan sesar menunjukkan perbedaan komposisi mikrobiomanya. Namun mikrobioma manusia tidak sepenuhnya stabil ke pola dewasa sampai usia 2-3 tahun. Teknologi baru dan teknik bioinformatika untuk analisis genom DNA mikroba yang diekstraksi dari sampel lingkungan memberikan wawasan di bidang ini yang sebelumnya tidak mungkin. Salah satu topik yang menarik adalah sifat interaksi nonpatogenik antara mikrobioma dalam ruangan dan manusia.
Studi neonatus memberikan bukti bahwa mikroba dari lingkungan yang berasal dari manusia dapat mempengaruhi mikrobioma manusia. Penelitian lain juga telah memberikan bukti bahwa anjing dan manusia memiliki bakteri yang sama. Namun tidak ada bukti nyata bahwa mikrobioma manusia dapat dijajah oleh bakteri yang berasal dari sebuah bangunan. Misalnya, studi mendalam tentang mikrobioma dalam ruangan dan manusia di mana tujuh keluarga diikuti selama 6 minggu menunjukkan bahwa mayoritas mikrobioma bangunan yang dapat diukur pada permukaan rumah berasal dari penghuninya.
Studi ini juga menemukan bahwa mikrobioma bangunan tampaknya tidak mempengaruhi struktur atau komposisi mikroba kulit penghuni. Penelitian lebih lanjut akan diperlukan untuk memahami reproduktifitas dan generalisasi dari temuan penelitian ini, dan bagaimana suhu, kelembaban, bahan bangunan, dan integritas struktur bangunan berdampak pada pertukaran antara mikrobioma bakteri dalam ruangan dan manusia.
Sumber Mikrobioma Dalam Ruangan Yang Relevan dengan Kesehatan Manusia
Pengamatan terbaru menunjukkan bahwa penghuni dan mikroba luar ruangan yang memasuki bangunan melalui ventilasi dan dilacak melalui debu adalah asal dominan bakteri lingkungan dalam ruangan, terutama yang dapat terbawa udara. Penghuni yang berkontribusi terhadap mikrobioma dalam ruangan termasuk manusia dan penghuni bukan manusia, seperti hewan pengerat dan kecoak, serta hewan peliharaan, yang merupakan sumber bakteri dan oleh karena itu dapat menjadi sumber langsung PAMP bakteri. Dalam studi peternakan, kemungkinan sumber untuk PAMP dalam ruangan termasuk pakan ternak dan hewan ternak.
Di lingkungan perkotaan, sumber LPS/endotoksin tidak hanya mencakup hewan peliharaan tetapi juga asosiasi dengan kelembaban, seperti yang disebabkan oleh ruang bawah tanah beton, pelembab udara , dan kerusakan akibat air pada situasi yang tidak terlalu ekstrim dibandingkan kondisi banjir. Endotoksin pada kotoran dan bahan tanaman yang membusuk dapat dilacak ke dalam rumah oleh penghuninya. Di sisi lain, kontribusi relatif partikel udara luar ruangan yang mengandung endotoksin atau mikroba ke rangkaian komponen mikroba dalam ruangan tidak dipahami dengan baik. Meskipun tidak kausal atau definitif, ada bukti bahwa paparan LPS/endotoksin dapat melindungi perkembangan alergi di lingkungan pedesaan ( Thorne, 2015 ) dan perkotaan AS.
Sumber jamur di dalam ruangan bervariasi. Biasanya, pada bangunan yang tidak rusak karena air, jamur masuk ke dalam bangunan melalui kebocoran pada selubung bangunan dan melalui sistem ventilasi, dibawa ke dalam ruangan oleh penghuninya, atau dapat dibawa ke dalam ruangan terkait dengan bahan bangunan. Pertumbuhan jamur umumnya tergantung pada kelembaban. Dalam kasus kerusakan air yang ekstrem seperti pada banjir di New Orleans, Louisiana di Cedar Rapids, Iowa atau di Boulder, Colorado tingkat tinggi jamur yang tidak berasal dari penghuni bangunan telah diukur pada permukaan bangunan dan di udara. Bahkan di bangunan yang tidak rusak karena air, jamur dapat tumbuh di dalam atau di atas bahan bangunan jika ada kelembaban yang cukup, dan pertumbuhannya dipengaruhi oleh faktor-faktor seperti komposisi kimia bahan bangunan. bahan bangunan.
National Academies of Sciences, Engineering, and Medicine. 2017. Microbiomes of the Built Environment: A Research Agenda for Indoor Microbiology, Human Health, and Buildings. Washington, DC: The National Academies Press.Tergantung pada kelembaban. Dalam kasus kerusakan air yang ekstrem—seperti pada banjir di New Orleans, Louisiana di Cedar Rapids, Iowa atau di Boulder, Colorado tingkat tinggi jamur yang tidak berasal dari penghuni bangunan telah diukur pada permukaan bangunan dan di udara. Bahkan di bangunan yang tidak rusak karena air, jamur dapat tumbuh di dalam atau di atas bahan bangunan jika ada kelembaban yang cukup, dan pertumbuhannya dipengaruhi oleh faktor-faktor seperti komposisi kimia bahan bangunan. bahan bangunan.
Kurang saat ini dipahami tentang asal-usul virus di lingkungan binaan (di luar transmisi patogen tertentu). Bukti menunjukkan, bagaimanapun, baik peningkatan sumber bakteri relatif terhadap virus di dalam ruangan atau penghilangan virus secara preferensial saat udara menembus di dalam ruangan.
Perlindungan Terhadap Orang yang Hidup Dengan Human Immunodeficiency Virus
Perlindungan Terhadap Orang yang Hidup Dengan Human Immunodeficiency Virus – Orang yang hidup dengan human immunodeficiency virus (PLWH) telah terpengaruh secara tidak proporsional oleh kolonisasi dan infeksi Staphylococcus aureus (MRSA) yang resistan terhadap methicillin, khususnya oleh klon USA300 dan USA500.
Perlindungan Terhadap Orang yang Hidup Dengan Human Immunodeficiency Virus

Baca Juga : Lanskap Peluang untuk Penelitian Ekologi Mikroba
hospitalmicrobiome – Namun, kontribusi faktor risiko epidemiologis, bakteri, dan imunologis terhadap kelebihan S aureus pada ODHA masih belum sepenuhnya dipahami.Dalam studi potong lintang ini, kami menentukan prevalensi dan epidemiologi molekuler kolonisasi S aureus pada 93 ODHA yang datang ke klinik human immunodeficiency virus (HIV) perkotaan. Peserta menyelesaikan wawancara terstruktur yang menilai informasi demografis dan faktor risiko MRSA. Swab diperoleh dari hidung, tenggorokan, dan selangkangan dan dikultur untuk S aureus dan Staphylococcus epidermidis .
Sebagian besar peserta memiliki infeksi HIV yang terkontrol dengan baik (89, 96% CD4 >200). Tiga puluh enam (39%) individu dikolonisasi dengan S aureus di 1 atau lebih bagian tubuh, termasuk 6 (6%) dengan MRSA. Penggunaan gym secara teratur merupakan faktor risiko S aureus tetapi bukan pembawa MRSA. Sebaliknya, S epidermidis hadir di hampir semua individu (n = 84, 90%), terutama di nares (n = 66, 71%). Menggunakan model persamaan perkiraan umum, kami mengamati bahwa kemungkinan kolonisasi S aureus berkurang secara signifikan dan drastis ketika S epidermidis terdeteksi ( P = .0001). Setelah mengontrol situs, jenis kelamin, dan usia, kami mengidentifikasi bahwa kemungkinan S aureuskolonisasi adalah 80% lebih sedikit jika S epidermidis hadir (rasio odds yang disesuaikan, 0,20; interval kepercayaan 95%, .09-.45; P <.0001).
Selama 15 tahun terakhir, infeksi Staphylococcus aureus resisten methicillin terkait komunitas (CA-MRSA) telah muncul berurutan untuk infeksi MRSA terkait perawatan kesehatan (HA ) . Akun MRSA terkait komunitas untuk sebagian besar infeksi kulit dan jaringan lunak (SSTI) di Amerika Serikat. Orang yang hidup dengan human immunodeficiency virus (ODHA) telah terpengaruh secara tidak proporsional oleh HA- dan CA-MRSA sebagaimana dibuktikan oleh peningkatan frekuensi kolonisasi S aureus , infeksi kulit, dan infeksi aliran darah invasif. Beberapa penelitian menunjukkan bahwa ODHA memiliki tingkat insiden S aureus 6–18 kali lebih tinggiinfeksi bila dibandingkan dengan kontrol negatif human immunodeficiency virus (HIV) yang sehat.
Peningkatan insiden infeksi S aureus kemungkinan multifaktorial dan mencakup faktor perilaku, imun pejamu, dan patogen. Telah terbukti bahwa penggunaan narkoba suntikan, tunawisma, aktivitas seksual berisiko tinggi, atau perpanjangan masa tinggal di rumah sakit dapat berkontribusi pada peningkatan beban ini Selain itu, defisiensi imun yang parah seperti yang dimanifestasikan oleh jumlah CD4 yang rendah secara signifikan berkontribusi pada hasil S aureus yang lebih buruk tetapi bahkan pada Odha yang menggunakan ART, insiden keseluruhan kolonisasi dan penyakit S aureus tetap meningkat secara signifikan.
Dalam pengaturan perawatan kesehatan, pengangkutan MRSA melalui hidung telah dikaitkan dengan infeksi MRSA berikutnya. Peran kolonisasi S aureus dan MRSA dalam infeksi berikutnya kurang jelas dalam pengaturan komunitas . Baru-baru ini, kolonisasi situs tubuh selain lubang hidung telah diakui sebagai reservoir potensial untuk menginfeksi strain S aureus, termasuk pada ODHA. Studi-studi ini juga menyarankan bahwa tipe klon tertentu seperti USA300 dan USA500 lebih disukai menjajah bagian tubuh tertentu seperti selangkangan, khususnya pada pasien yang terinfeksi HIV. Ini menunjukkan kemungkinan interaksi spesifik antara sistem kekebalan yang terganggu setelah infeksi HIV dan susunan molekul klon S aureus yang berbeda. Pasien dengan infeksi HIV, bahkan ketika dalam terapi antiretroviral, tampaknya memiliki defek persisten pada respon imun yang diperantarai Th17, yang sangat penting dalam mengendalikan infeksi S aureus. Selain itu, peningkatan respon Th2 secara bersamaan dan aktivasi imun kronis dapat menyebabkan downregulasi peptida antimikroba human -defensin (hBD)2 dan hBD3, yang juga penting dalam respon keratinosit terhadap S aureus.
Selain faktor inang, kolonisasi S aureus juga ditentukan oleh interaksi dengan mikrobiota lokal. Telah disarankan bahwa Staphylococcus epidermidis komensal yang sering khususnya memiliki kemampuan untuk secara langsung menghambat kolonisasi S aureus dengan sekresi protease serin, Esp1, atau dengan aktivasi Toll-like receptor-2 pada keratinosit, memicu pelepasan peptida antimikroba. Pentingnya interaksi ini pada pasien dengan HIV masih belum diketahui.Selain faktor inang, kolonisasi S aureus juga ditentukan oleh interaksi dengan mikrobiota lokal. Telah disarankan bahwa Staphylococcus epidermidis komensal yang sering khususnya memiliki kemampuan untuk secara langsung menghambat kolonisasi S aureus dengan sekresi protease serin, Esp1, atau dengan aktivasi Toll-like receptor-2 pada keratinosit, memicu pelepasan peptida antimikroba. Pentingnya interaksi ini pada pasien dengan HIV masih belum diketahui.
Studi Populasi
Studi cross-sectional ini ditinjau dan disetujui oleh Dewan Peninjau Institusional Universitas Columbia Medical Center (New York, NY). Penelitian berlangsung pada bulan Januari dan Februari 2013 di klinik Program HIV Komprehensif Presbyterian New York. Pasien diberitahu tentang studi oleh penyedia perawatan primer mereka dan, setelah memberikan persetujuan lisan untuk dihubungi, didekati oleh tim studi. Setelah memberikan persetujuan tertulis, pasien direkrut ke dalam penelitian. Secara total, 96 pasien memenuhi kriteria inklusi sebagai HIV positif dan berusia 18 tahun; 93 pasien menyelesaikan survei dan memberikan semua penyeka situs tubuh. Pasien yang datang ke klinik tidak memenuhi syarat untuk berpartisipasi jika status HIV mereka negatif atau tidak diketahui (n = 1); atau jika mereka memiliki penyakit radang usus (n = 1). Kriteria eksklusi lain yang ditentukan sebelumnya dari infeksi oportunistik yang menentukan sindrom defisiensi imun akut atau didapat dalam waktu 4 minggu sebelum masuk penelitian atau penggunaan obat imunosupresif sistemik saat ini (misalnya, kortikosteroid) dalam waktu 14 hari sebelum masuk penelitian tidak ditemukan. Peserta diberi kompensasi dengan kartu hadiah $10 ke CVS Pharmacy.
survei
Pasien menyelesaikan wawancara terstruktur menggunakan perangkat lunak wawancara mandiri dengan bantuan komputer audio. Pertanyaan menilai informasi demografis dan faktor risiko MRSA, termasuk kebiasaan perawatan pribadi, serta aspek terkait dari riwayat medis, sosial, dan seksual. Selain itu, tinjauan retrospektif dari catatan medis pasien dilakukan untuk memastikan informasi klinis dan laboratorium yang relevan. Ini juga termasuk penilaian penyakit kulit yang mendasari (eksim, psoriasis, dermatitis seboroik, dermatitis lichenoid, alergi kulit, jerawat, tinea, karsinoma sel basal, dan zoster) atau infeksi kulit dan jaringan lunak dan infeksi oportunistik dan paparan antibiotik selama 3 bulan sebelumnya. pendaftaran.
Pengumpulan Sampel Mikrobiologi dan Studi Molekuler
Setelah menyelesaikan survei, hidung, tenggorokan, dan selangkangan peserta diambil sampelnya menggunakan swab steril yang telah dibasahi sebelumnya (BD BBL CultureSwab; BD Diagnostic Systems, Sparks, MD). Situs kulit tambahan diambil sampelnya jika peserta penelitian melaporkan kemungkinan lesi kulit yang terinfeksi. Sampel diproses seperti yang dijelaskan sebelumnya . Singkatnya, biakan swab diinkubasi semalaman pada suhu 37 ° C dalam kaldu kedelai Tryptic 6% yang ditambah garam dan dilapisi ke agar garam Mannitol (Becton Dickinson, Sparks, MD). Koloni kuning positif yang memfermentasi manitol diisolasi pada 5% darah domba/piring agar kedelai Tryptic (darah/TSA) (Becton Dickinson). Stafilokokus aureusdiidentifikasi dari darah/TSA oleh koagulase dan kit deteksi Protein A (Murex StaphAurex). Selain itu, semua koloni nonmanitol-fermenting dan Staphaurex-negatif diisolasi ke TSA (Becton Dickinson, Sparks, MD). Staphylococcus epidermidis diidentifikasi dari TSA dengan reaksi rantai polimerase spesifik spesies (PCR) seperti yang dijelaskan sebelumnya.
Semua isolat S aureus digenotipe dengan pengurutan dan analisis daerah-ulang protein stafilokokus A ( spa ) (Ridom-staphsoftware). Keterkaitan regangan dievaluasi lebih lanjut menggunakan algoritma pola ulangan berbasis terintegrasi (BURP) untuk clustering Spa Clonal Complex ( spa -CCs). Kehadiran dan jenis Mec Kaset Kromosom Stafilokokus (SCC) , ditentukan dengan PCR multipleks, digunakan untuk mengevaluasi resistensi methicillin. Isolat selanjutnya digenotipe dengan menguji keberadaan gen arginine-catabolic mobile element (ACME) dengan PCR.Semua isolat S epidermidis diuji keberadaan gen serin protease esp dengan PCR. Untuk pengujian kerentanan antibiotik, kami secara acak memilih 1 isolat S epidermidis per peserta dari setengah dari individu yang dijajah S epidermidis , karena kendala biaya. Isolat diuji resistensinya terhadap penisilin, levofloksasin, gentamisin, eritromisin, linezolid, tetrasiklin, cefoxitin, dan rifampisin menggunakan metode Kirby-Bauer dan standar Clinical and Laboratory Standards Institute (CLSI ) .
Analisis Statistik
Semua analisis statistik dilakukan dengan menggunakan SAS 9.4 (SAS Institute Inc., Cary, NC). Kami menguji 2 hasil terpisah terhadap setiap faktor risiko yang dihipotesiskan: kolonisasi dengan S aureus (S aureus sensitif methicillin [MSSA] atau MRSA) di bagian tubuh mana pun atau kolonisasi dengan MRSA di bagian tubuh mana pun. Perbandingan peserta yang terjajah dengan yang tidak terjajah pada variabel dikotomis dilakukan dengan menggunakan 2 atau uji eksak Fisher jika sesuai. Analisis bivariat dengan prediktor kontinu dievaluasi menggunakan uji t Student tidak berpasangan. Persamaan estimasi umum (GEEs) digunakan untuk mengevaluasi hubungan antara S aureus dan S epidermidiskolonisasi. Metode ini memungkinkan kami untuk mengontrol beberapa usap bagian tubuh yang diambil per individu. Semua uji statistik adalah 2 sisi, dengan P < 0,05 dianggap signifikan. Studi Demografi dan Prevalensi Kolonisasi Penelitian cross-sectional ini melibatkan 93 peserta HIV-positif dengan usia rata-rata 50 tahun (kisaran interkuartil, 44-60). Sekitar sepertiga dari populasi adalah perempuan (n = 32, 34%), dua pertiga adalah laki-laki (n = 60, 65%), dan 1 individu adalah transgender (n = 1, 1%; Tabel 1). Hispanik (n = 44, 48%) dan Afrika Amerika (n = 34, 37%) terdiri dari kelompok etnis terbesar dalam penelitian kami, sedangkan kulit putih (n = 9, 10%) dan ras lain (n = 5, 5%) lebih jarang diwakili. Mayoritas peserta mengidentifikasi diri sebagai heteroseksual (n = 55, 59%); sepertiga (n = 31, 33%) mengidentifikasi diri sebagai laki-laki yang berhubungan seks dengan laki-laki (50% laki-laki). Sebagian besar peserta memiliki infeksi HIV yang terkontrol dengan baik karena 89 orang (96%) memiliki jumlah CD4 baru-baru ini >200 dan viral load tidak terdeteksi pada kunjungan terakhir mereka. Hanya 4 pasien yang memiliki viral load baru-baru ini >1000. Beberapa peserta (n = 5, 5%) dirawat di rumah sakit dalam 3 bulan sebelumnya partisipasi studi.
Karakterisasi Molekuler dan Fenotipik
Di antara 36 individu yang dijajah, kami mengamati 26 jenis spa yang berbeda . Dari 14 individu yang berkoloni di beberapa bagian tubuh, hanya 1 yang memiliki tipe spa yang berbeda di 3 bagian tubuh yang diuji. Sebagian besar isolat yang berkoloni adalah MSSA (86%) dan termasuk dalam keragaman tipe spa. Jenis spa yang paling sering adalah t002, terhitung 15% dari isolat MSSA. Setengah dari isolat MRSA adalah spa type t008, konsisten dengan USA300. Enam dari 8 isolat MRSA (75%) adalah ACME positif, konsisten dengan USA300. Kami mengamati spa -type t064 pada kelompok MSSA dan MRSA.
Staphylococcus epidermidis telah dikaitkan dengan resistensi antibiotik yang substansial. Uji kepekaan antibiotik pada subset koleksi S epidermidis menunjukkan bahwa hampir semua isolat resisten terhadap penisilin (n = 40, 93%; Gambar 2 ). Hanya 12% (n = 5) yang resisten terhadap cefoxitin, konsisten dengan S epidermidis yang resisten methicillin. Strain S epidermidis yang resisten methicillin lebih cenderung tidak peka terhadap tetrasiklin dibandingkan dengan kelompok S epidermidis yang sensitif methicillin (masing-masing 80% vs 13%; Fisher’s exact test, P= .005). Kedua kelompok tidak memiliki perbedaan yang signifikan dalam kerentanan antibiotik, dan semua isolat rentan terhadap linezolid, rifampisin, dan vankomisin. Semua isolat S epidermidis diketik untuk gen esp dan positif.
Lanskap Peluang untuk Penelitian Ekologi Mikroba
Lanskap Peluang untuk Penelitian Ekologi Mikroba – Mikroba mencakup keanekaragaman hayati yang luar biasa, memberikan dukungan bagi semua bentuk kehidupan, termasuk manusia, dan memainkan peran penting dalam banyak jasa ekosistem.
Lanskap Peluang untuk Penelitian Ekologi Mikroba
Baca Juga : Mempelajari Mikrobiologi Lingkungan Dalam Ruangan
hospitalmicrobiome – Aturan yang mengatur perakitan komunitas mikroorganisme semakin terungkap karena kemajuan utama dalam metode molekuler dan analitik tetapi pemahaman mereka tetap menjadi tantangan utama dalam ekologi mikroba. Keberadaan pola biogeografi dalam komunitas mikroba telah ditetapkan dan dijelaskan dalam kaitannya dengan proses skala lanskap, termasuk seleksi, drift, penyebaran dan mutasi. Pengaruh tambal sulam habitat pada aturan perakitan mikroorganisme tetap ada meskipun tidak sepenuhnya dipahami. Di sini, kami meninjau bagaimana prinsip-prinsip ekologi lanskap dapat diadaptasi untuk mengeksplorasi perspektif baru tentang mekanisme yang menentukan struktur komunitas mikroba.
Untuk memberikan gambaran umum, kami mengkarakterisasi lanskap mikroba, skala spasial dan temporal dari mekanisme yang mendorong perakitan mikroba dan umpan balik antara mikroorganisme dan struktur lanskap. Kami memberikan bukti untuk efek heterogenitas lanskap, fragmentasi lanskap, dan dinamika lanskap pada struktur komunitas mikroba, dan menunjukkan bahwa prediksi yang dibuat untuk organisme makro setidaknya sebagian juga berlaku untuk mikroorganisme. Kami menjelaskan mengapa pendekatan komunitas meta yang muncul dalam ekologi mikroba harus mencakup karakterisasi eksplisit struktur lanskap dalam pengembangan dan interpretasinya. Kami juga menjelaskan bagaimana interaksi biotik, seperti kompetisi, mangsa-predator atau hubungan mutualis dapat mempengaruhi lanskap mikroba dan mungkin terlibat dalam proses umpan balik yang disebutkan di atas. Namun, kami berpendapat bahwa penerapan ekologi lanskap ke dunia mikroba tidak bisa begitu saja melibatkan pemindahan kerangka teoretis yang ada.
Ini karena kekhasan organisme ini, dalam hal ukuran, waktu generasi, dan untuk beberapa di antaranya, interaksi yang erat dengan inang. Karakteristik ini menyiratkan berurusan dengan ruang dan skala waktu efek yang tidak biasa dan bergantung. Proses evolusi juga sangat penting dalam respons mikroorganisme terhadap lanskap mereka. Terakhir, aktivitas dan distribusi mikroorganisme menyebabkan efek umpan balik pada lanskap yang harus diperhitungkan. Transposisi kerangka ekologi lanskap ke mikroorganisme memberikan banyak arah penelitian yang menantang untuk ekologi mikroba. Ini karena kekhasan organisme ini, dalam hal ukuran, waktu generasi, dan untuk beberapa di antaranya, interaksi yang erat dengan inang.
Karakteristik ini menyiratkan berurusan dengan ruang dan skala waktu efek yang tidak biasa dan bergantung. Proses evolusi juga sangat penting dalam respons mikroorganisme terhadap lanskap mereka. Terakhir, aktivitas dan distribusi mikroorganisme menyebabkan efek umpan balik pada lanskap yang harus diperhitungkan. Transposisi kerangka ekologi lanskap ke mikroorganisme memberikan banyak arah penelitian yang menantang untuk ekologi mikroba. Ini karena kekhasan organisme ini, dalam hal ukuran, waktu generasi, dan untuk beberapa di antaranya, interaksi yang erat dengan inang. Karakteristik ini menyiratkan berurusan dengan ruang dan skala waktu efek yang tidak biasa dan bergantung.
Proses evolusi juga sangat penting dalam respons mikroorganisme terhadap lanskap mereka. Terakhir, aktivitas dan distribusi mikroorganisme menyebabkan efek umpan balik pada lanskap yang harus diperhitungkan. Transposisi kerangka ekologi lanskap ke mikroorganisme memberikan banyak arah penelitian yang menantang untuk ekologi mikroba. Proses evolusi juga sangat penting dalam respons mikroorganisme terhadap lanskap mereka. Terakhir, aktivitas dan distribusi mikroorganisme menyebabkan efek umpan balik pada lanskap yang harus diperhitungkan.
Transposisi kerangka ekologi lanskap ke mikroorganisme memberikan banyak arah penelitian yang menantang untuk ekologi mikroba. Proses evolusi juga sangat penting dalam respons mikroorganisme terhadap lanskap mereka. Terakhir, aktivitas dan distribusi mikroorganisme menyebabkan efek umpan balik pada lanskap yang harus diperhitungkan. Transposisi kerangka ekologi lanskap ke mikroorganisme memberikan banyak arah penelitian yang menantang untuk ekologi mikroba.
Mikroorganisme merupakan bagian terbesar dari keanekaragaman hayati. Ada 100 juta kali lebih banyak bakteri di lautan (13 × 10 2 8) daripada jumlah bintang di alam semesta yang diketahui [Editorial Nature Review in Microbiology,. Kelimpahan yang menakjubkan dari mikroorganisme di bumi memainkan peran sentral dalam siklus biogeokimia unsur , mempengaruhi kesuburan tanah, dekomposisi bahan organik dan penyimpanan karbon.
Mikroorganisme juga diperlukan untuk menopang semua makroorganisme hidup, termasuk manusia , karena mereka terlibat dalam nutrisi, kesehatan, reproduksi, dan perilaku inangnya. Akibatnya, mereka memastikan sebagian besar layanan ekosistem diberikan kepada masyarakat kita. Namun, mikroorganisme menunjukkan heterogenitas spasial yang substansial. Hal ini menimbulkan pertanyaan tentang bagaimana distribusi mikroba tergantung pada komponen yang berbeda dari perakitan komunitas, hubungannya dengan teori niche dan mekanisme koeksistensi, dan bagaimana perakitan komunitas terkait dengan fungsi dan fungsi ekosistem mikroba ini.
Penggerak kumpulan mikroorganisme sejauh ini sebagian besar telah dianalisis pada skala patch, dengan asumsi bahwa relung spesies dihasilkan dari pengaruh lingkungan abiotik pada pemilihan spesies, gangguan atau interaksi biotik di antara organisme mikroba, atau dengan inangnya dan mengabaikan efek penyebaran. Karena mikroorganisme memiliki kapasitas reproduksi yang sangat tinggi dan waktu generasi yang singkat, pandangan historis “ segala sesuatu ada di mana-mana tetapi lingkungan memilih ” telah diterima sejak lama. Kemajuan dalam resolusi komposisi komunitas mikroba yang diperoleh dari sekuensing massal dan studi distribusi mikroba skala besar memberikan peningkatan jumlah bukti bahwa mikroorganisme jauh lebih terbatas dalam penyebarannya daripada yang diduga sebelumnya. Kerangka kerja berdasarkan biogeografi skala besar telah berhasil digunakan untuk memahami pola spasial spesies dalam skala besar.
Kerangka kerja ini menganggap bahwa perakitan komunitas di patch lokal yang dianggap sebagai “pulau” hasil dari proses kolonisasi dan kepunahan, kedua proses tersebut terkait dengan ukuran dan jarak patch ke sumber patch (“benua”). Pendekatan implisit spasial yang dibangun di atas teori biogeografi pulau dari MacArthur dan Wilson (1967) adalah titik awal yang berguna untuk mempertimbangkan bagaimana penyebaran dapat mempengaruhi perakitan komunitas di tingkat lanskap, dimulai pada satu spesies, untuk berkumpul dengan beberapa spesies. Metakomunitas terdiri dari kumpulan komunitas yang terhubung melalui penyebaran. Dengan demikian, empat proses utama dapat mendorong variasi komunitas dalam ruang, yaitu seleksi spesies (termasuk faktor abiotik dan biotik), spesiasi (analog dengan mutasi dalam genetika populasi), penyebaran dan pergeseran ekologis.
Pendekatan alternatif untuk dinamika spasial dalam ekologi muncul sekitar 30 tahun yang lalu dalam bentuk ekologi lanskap. Ekologi lanskap berfokus secara khusus pada analisis eksplisit pola ekologi spasial dan telah menentukan konseptualisasi apa itu lanskap , dan menyediakan alat untuk menganalisis bagaimana proses spasial memengaruhi kumpulan keanekaragaman hayati, dengan fokus terutama pada tumbuhan dan hewan. Struktur lanskap, dijelaskan melalui metrik yang berbeda pada skala lanskap (yaitu, heterogenitas) atau skala habitat (yaitu, fragmentasi), telah terbukti mempengaruhi penyebaran, dan eksploitasi habitat lokal selama siklus hidup organisme, tetapi juga ketersediaan habitat untuk spesies perkembangan dan pergerakan antar patch lokal . Kedua jenis metrik ini – heterogenitas lanskap dan fragmentasi mempengaruhi kelimpahan dan komposisi spesies. Namun, penelitian ekologi lanskap sebagian besar terkonsentrasi pada makroorganisme dan kompartemen mikroba tetap dipelajari di bawah kerangka kerja ini.
Menerapkan prinsip-prinsip ekologi lanskap untuk mikroorganisme, sampai saat ini, lambat berkembang karena pemahaman kami yang terbatas tentang persyaratan habitat mikroba, kesulitan yang terlibat dalam mengamati pergerakan mikroorganisme dan kapasitas kami yang terbatas untuk melakukan survei luas distribusi mikroba. Penentuan komposisi komunitas mikroba juga sulit karena komunitas mikroba bisa sangat kompleks dan perlu dipelajari dengan pendekatan sekuensing massal.
Dari sifat data yang digunakan, penggambaran urutan spesies mikroba juga diperlukan dan adopsi konsep spesies filogenetik yaitu, “ kelompok organisme individu terkecil yang dapat didiagnosis di mana terdapat pola nenek moyang dan keturunan. ” tersirat. Setelah menggunakan cutoff identitas urutan untuk mengidentifikasi Unit Taksonomi Operasional, kemajuan bioinformatika terbaru sekarang memungkinkan menghindari penggunaan cutoff buatan ini yaitu, cluster-urutan dan Varian Urutan Amplicon dan tentukan taksa pada butir yang lebih tipis. Resolusi yang lebih baik dalam deskripsi komunitas ini memberikan dasar untuk menguji konsep ekologi baru seperti ekologi lanskap. Penerapan ekologi lanskap ke dunia mikroba juga membutuhkan karakterisasi lanskap di mana mikroba hidup.
Lanskap tersebut dapat berupa kumpulan tipe habitat yang berbeda dengan kondisi lingkungan yang bervariasi, tetapi juga dapat menjadi kumpulan inang yang tersedia untuk kolonisasi mikroba. Lanskap “biotik” ini kemudian dapat didorong oleh perilaku dan pertumbuhan organisme makro yang menjadi inang bagi mikroorganisme, dan bergantung pada respons inang ini terhadap karakteristik lanskap mereka sendiri. Terakhir, lanskap mikroba dapat berada di dalam inang, sesuai dengan situs anatomi yang berbeda di dalam tubuh, dan bahkan di dalam setiap organ, memberikan tambalan yang bervariasi dalam kondisi lingkungannya. Selain itu, mikroorganisme individu berinteraksi dengan fitur dan volume permukaan nano dan mikro. Lanskap skala kecil yang tidak biasa harus dipertimbangkan karena ukuran mikroorganisme yang sangat kecil.
Dalam lanskap skala mikro ini seperti di lingkungan terestrial atau perairan, distribusi mikroorganisme terkait erat dengan heterogenitas patch. Namun, sebagian besar penulis tidak mendasarkan pekerjaan mereka dalam kerangka ekologi lanskap, dan baru-baru ini ekologi mikroba mengembangkan integrasi eksplisit prinsip-prinsip ekologi lanskap untuk memahami pendorong distribusi mikroba. Karena kekhususan mikroba ini definisi spesies, penyebaran, respons terhadap heterogenitas biotik, dan respons skala kecil terhadap lingkungan transposisi kerangka teoretis yang ada dalam ekologi lanskap untuk menganalisis aturan perakitan mikroorganisme kemungkinan tidak langsung.
Tujuan dari tinjauan ini adalah untuk menyelidiki bagaimana konsep ekologi lanskap dapat diterapkan pada dunia mikroba, untuk memajukan pemahaman kita tentang dunia ini dan untuk menunjukkan bagaimana mikroorganisme dapat digunakan sebagai model baru untuk menguji dan memperluas kerangka ekologi lanskap yang ada. Kami memperhitungkan ekosistem perairan, daratan, dan laut, serta semua jenis interaksi mikrobiota inang, mulai dari mikroorganisme yang hidup bebas hingga mikroorganisme yang terkait dengan tanaman, hewan, dan manusia. Virus dikeluarkan dari ruang lingkup makalah karena ukurannya yang sub-mikroskopis. Jika ada alasan kuat tentang pentingnya virus untuk asal usul sel dan diversifikasi, ada bukti yang menentang gagasan bahwa virus itu hidup. Penyebaran, perubahan genetik, dan perbanyakan mereka ditentukan oleh batasan spesifik yang tidak dikembangkan di sini.
Distribusi spesies dapat dikaitkan dengan ketidakrataan lingkungan melalui cara kondisi abiotik (atau biotik) didistribusikan di ruang angkasa. Konsekuensi dari ketidakrataan lingkungan tersebut pada proses ekologi termasuk perakitan spesies dapat dianalisis menggunakan model konseptual lanskap yang berbeda . Model konseptual pertama, dan sederhana yang diturunkan dari teori biogeografi pulau, menganggap bahwa patch habitat yang identik (yaitu, sesuai dengan relung yang menguntungkan) tertanam dalam matriks non-habitat yang berbeda.
Dalam pandangan pertama ini, lanskap dicirikan oleh metrik yang mengkuantifikasi jumlah patch yang menguntungkan atau isolasinya, dengan anggapan bahwa lanskap lainnya tidak bertindak berdasarkan kumpulan spesies. Model patch-matrix kemudian dengan cepat diperluas ke model lanskap mosaik dengan memasukkan mosaik habitat yang terdiri dari lanskap, dan yang dapat dianggap terdiri dari habitat yang kurang lebih menguntungkan untuk pengembangan. Spesies memang berpotensi bergantung pada patch habitat yang berbeda untuk siklus hidup mereka sebagai contoh untuk hewan, yang tahap juvenilnya bergantung pada satu tipe habitat tertentu dan tahap dewasa pada yang lain. Mereka juga dapat mengandalkan habitat alternatif untuk perkembangan mereka .
Mosaik bentuk patch juga menyebar dengan bertindak pada permeabilitas lanskap terhadap pergerakan spesies. Dalam visi kedua ini, lanskap dicirikan oleh metrik yang mengukur heterogenitasnya dalam hal komposisi patch, yang menentukan jenis, kekayaan, dan kelimpahan relatif dari patch yang berbeda. Heterogenitas konfigurasi mendefinisikan pengaturan dalam ruang patch yang berbeda dan terkait dengan metrik yang mengukur fitur seperti ukuran patch, agregasi, jenis antarmuka di antara patch. Model konseptual terakhir baru-baru ini muncul, model kontinum, mengingat lanskap adalah kombinasi dari beberapa gradien lingkungan yang berkelanjutan alih-alih tambalan diskrit. Untuk model ini, metrik yang digunakan untuk menggambarkan lanskap bersifat kontinu, dan dapat mengintegrasikan sebagian respons spesies terhadap gradien lingkungan ini melalui, misalnya, tingkat kesesuaian antara kondisi abiotik dan persyaratan ekologi spesies.
Sebagian besar studi mikroba berdasarkan ekologi lanskap didasarkan pada model matriks-tambalan, sedangkan model mosaik hanya digunakan dalam kasus-kasus tertentu di mana tambalan sangat heterogen, atau di mana tambalan diskrit sesuai dengan inang yang berbeda. Korelasi antara faktor lingkungan dan komposisi komunitas mikroba telah dipelajari secara ekstensif . Meskipun umumnya menyiratkan model konseptual kontinum, pola-pola ini belum terhubung dengan baik ke teori yang mendasari di balik model konseptual lanskap. Kami meninjau bukti efek lanskap yang ada di bagian “Pengaruh Heterogenitas Mosaik Lanskap dan Fragmentasi Habitat pada Mikroorganisme” di bawah ini.
Mempelajari Mikrobiologi Lingkungan Dalam Ruangan
Mempelajari Mikrobiologi Lingkungan Dalam Ruangan – Mayoritas orang di negara maju menghabiskan lebih dari 90% hidup mereka di dalam ruangan. Di sini, kami memeriksa pemahaman kami tentang bakteri yang menghuni dunia buatan kami dan bagaimana mereka dapat memengaruhi kesehatan manusia.
Mempelajari Mikrobiologi Lingkungan Dalam Ruangan
Baca Juga : Mikroba Usus Mungkin Menjadi Kunci untuk Mengatasi Alergi Makanan
hospitalmicrobiome – Tren global menuju industrialisasi dan urbanisasi telah menyebabkan semakin banyak orang tinggal dan bekerja di dalam ruangan. Beberapa penelitian memperkirakan bahwa manusia di negara-negara industri menghabiskan sebanyak 90% dari hidup mereka di dala. Mereka lahir di rumah sakit, dibesarkan di rumah atau apartemen, bekerja di gedung perkantoran atau pabrik dan pindah ke panti jompo di hari tua mereka. Tren menuju kehidupan dalam ruangan ini juga terjadi di negara-negara berkembang. Tiga puluh tahun yang lalu, kota Shenzhen di Cina adalah kota kecil berpenduduk 300.000 jiwa. Sejak itu, telah berkembang menjadi megalopolis industri besar yang menampung lebih dari 10 juta orang, banyak dari mereka telah pindah ke sana dari daerah pedesaan . Jadi, bagi miliaran manusia, lingkungan buatan (BE) sekarang mewakili habitat ekologis modern Homo sapiens sapiens .
Dalam proses pembuatan BE, kita juga secara tidak sengaja telah menciptakan keragaman habitat mikro yang luar biasa yang telah dijajah oleh ribuan mikroorganisme yang berbeda. Memang, BE mengandung banyak habitat baru yang potensial untuk kehidupan mikroba yang memiliki sifat kimia dan fisik yang tidak ditemukan di alam. Manusia membawa sebagian besar mikroba yang mengkolonisasi ke habitat ini dengan cara melepaskannya dari tubuhnya atau mengangkutnya dengan pakaian dan sepatu, sedangkan sisanya berasal dari air atau sumber lingkungan lainnya (misalnya, tanah). Tergantung pada lingkungan, mikroba juga dapat diangkut di dalam ruangan oleh hewan peliharaan, serangga, dan hewan lain.
Sementara studi berbasis kultur telah menemukan mikroba ada di mana-mana di BE, studi molekuler independen budaya baru-baru ini telah menunjukkan bahwa pemahaman kita tentang keragaman mikroba dalam ruangan tetap sangat jarang. Metode molekuler ini juga merupakan bagian integral dari kit alat untuk memperluas pemahaman kita tentang spesies mikroorganisme apa yang hidup di ekosistem ini, bagaimana fungsinya dan bagaimana mereka bermigrasi di antara manusia, permukaan fisik, dan lingkungan lainnya.
Pendekatan molekuler yang paling umum digunakan untuk mengeksplorasi keragaman mikroba didasarkan pada amplifikasi PCR dan pengurutan gen yang mengkode RNA ribosom subunit kecil (16S rRNA) langsung dari sumber lingkungan. Dalam pendekatan ini, DNA diekstraksi langsung dari semua sel mikroba yang ada dalam sampel dan primer PCR ‘universal’ yang dirancang dari daerah yang dilestarikan dari gen 16S rRNA digunakan untuk mengamplifikasi gen ini dari semua genom mikroba dalam sampel. Pendekatan ini dengan mudah menentukan beberapa kali lipat lebih banyak keragaman mikroba daripada metode berbasis kultur, sering kali menemukan organisme baru tanpa kondisi pertumbuhan yang diketahui, dan telah secara dramatis mengubah pemahaman kita tentang keragaman mikroba global. Meskipun kuat, ada dua sumber bias yang jelas dalam metode ini.
Pertama, teknik ekstraksi DNA yang berbeda memungkinkan akses ke bagian yang berbeda dari keragaman mikroba pada tingkat yang bervariasi, melalui lisis sel yang tidak merata . Kedua, tidak ada primer PCR yang benar-benar universal, bahkan dengan pasangan yang paling komprehensif mencakup sekitar 85% dari taksa yang diketahui. Terlepas dari keterbatasan ini, teknologi ini, bila dikombinasikan dengan desain eksperimental yang ketat, sangat berguna untuk mengkarakterisasi dinamika dan pola ekologi ekosistem mikroba. Studi keragaman rRNA 16S awal dilakukan dalam amplikon PCR kloning BE ke dalam vektor plasmid sebelum transformasi, isolasi koloni dan pengurutan. Namun, penerapan sekuensing berbasis PCR langsung pada tahun 2006 secara dramatis meningkatkan kedalaman dan luasnya analisis; teknologi serupa sekarang memungkinkan pemrosesan simultan dari ribuan sampel pada kedalaman ratusan ribu urutan pembacaan setiap.
Di sini, kami meninjau literatur tentang analisis budaya independen keragaman mikroba di BE dan mengeksplorasi apa yang dikatakannya tentang dinamika dan distribusi bakteri dan jamur di lingkungan ini. Jadi, mengapa BE layak untuk ditelusuri? Pertama, seperti yang telah dinyatakan, BE adalah habitat utama bagi sebagian besar umat manusia yang terus berkembang, yang kesehatannya mungkin bergantung pada pemahaman kita yang kuat tentang interaksi antara manusia dan mikrobiologi bangunan. Kedua, iklim, bahan, dan desain lingkungan buatan dapat memiliki konsekuensi yang tidak terduga dan menarik bagi pemilihan dan pertumbuhan mikroba yang mungkin membantu kita merancang bangunan yang lebih sehat.
Akhirnya, pemahaman yang lebih dalam tentang keragaman mikroba dalam ruangan akan membantu menginformasikan kebijakan kesehatan masyarakat, terutama dalam pengaturan dengan banyak individu dengan gangguan kekebalan (misalnya, rumah sakit, unit perawatan intensif dan panti jompo). Minat baru dalam ekologi mikroba, dan penerapan teknologi pengurutan generasi berikutnya, menghadirkan peluang menarik untuk mengungkap keragaman dan interaksi tersembunyi di lingkungan ini. Seperti yang akan kami tunjukkan, metode-metode ini telah mengungkapkan BE sebagai ekosistem mikroba yang sangat kompleks dan sangat dinamis yang mengumpulkan dan memilih rangkaian keragaman baru yang luar biasa.
Tak perlu dikatakan bahwa BE mengandung senyawa kimia dan kondisi fisik yang sama sekali tidak seperti dunia alami di mana mikroba berevolusi. Dinding kering, lilin lantai, poliester, karpet, suhu dan kelembaban konstan, hidrokarbon dan polimer baru ini hanya beberapa dari banyak fitur yang ditemukan di BE yang berpotensi memberikan kondisi pertumbuhan dan relung yang tidak biasa untuk bakteri dan jamur. Sementara evolusi mikroba alami mungkin awalnya tidak memilih fenotipe yang dapat mengeksploitasi kondisi atau bahan ini, keragaman dan kemampuan beradaptasi yang luar biasa dari dunia mikroba berarti bahwa mungkin ada mikroba yang akan bertahan hidup di hampir semua permukaan atau kondisi BE. Selain itu, waktu generasi yang singkat dan mekanisme evolusi yang cepat (misalnya,
Studi berbasis kultur telah berulang kali menemukan kondisi di BE yang memperkaya bakteri dan jamur tertentu. Namun, sementara isolasi kultur berfokus pada keberadaan bakteri atau jamur tertentu, studi molekuler BE biasanya mengungkap komunitas polimikrobial yang terdiri dari ratusan atau ribuan mikroba yang tidak dikultur. Ketika kondisi di BE sangat memperkaya sifat-sifat tertentu, komunitas polimikrobial ini cenderung didominasi oleh beberapa kelompok mikroba. Misalnya, analisis keragaman urutan 16S rRNA bakteri di kolam terapi rumah sakit dan pancuran menemukan bahwa mereka diperkaya untuk beragam, terutama tidak berbudaya, Mycobacteria yang tinggal di tanah., serta banyak Proteobacteria dan kelompok lain yang lebih jarang. Tirai shower cenderung didominasi oleh lusinan spesies Sphingomonas dan Methylobacterium yang berbeda , banyak di antaranya tidak berbudaya.
Yang terakhir ini sangat menarik karena beberapa spesies Methylobacterium telah terbukti tumbuh pada keragaman yang sangat besar dari senyawa karbon yang berbeda (yaitu, senyawa C2, C3 dan C4), dan beberapa spesies berkembang pada produk peluruhan sel kulit manusia. Studi pancuran dan bilik pancuran rumah sakit menemukan mereka, seperti kolam terapi, menjadi lingkungan yang ramah untuk Actinobacteria dan Proteobacteria . Lingkungan sangat selektif lainnya termasuk selang kateter , yang mempertahankan komunitas mikroba yang berbeda secara signifikan secara internal dibandingkan dengan eksternal, dan ruang bersih NASA yang digunakan untuk perakitan pesawat ruang angkasa. Dalam kasus terakhir, protokol penyegelan dan sterilisasi ekstensif tampaknya hanya memilih mikroba yang paling kuat yang juga bertahan dalam perjalanan ruang angkasa .
Studi molekuler juga telah meningkatkan pemahaman kita tentang bagaimana mikroba dalam ruangan menjajah permukaan dan ditransmisikan di antara lingkungan mikro. Studi tentang keyboard, toilet dan kantor menunjukkan bahwa manusia adalah sumber utama keanekaragaman mikroba di banyak lingkungan dalam ruangan dan juga merupakan vektor prinsipnya. Mungkin tidak mengejutkan, sejumlah besar mikroba permukaan dapat ditelusuri kembali ke kulit manusia, meskipun usus dan lingkungan hidung/mulut juga berkontribusi. Studi molekuler keanekaragaman bakteri di kantor, rumah sakit, pesawat terbang , dapur dan toilet secara konsisten menemukan dominasi bakteri terkait kulit manusia, dan gastrointestinal atau urogenital, pada sebagian besar permukaan fisik. Faktanya, Tringe dan rekan menunjukkan bahwa bakteri yang hidup di kulit individu yang menghuni ruang tertentu menentukan komunitas mikroba yang diamati dalam sampel udara yang diambil dari ruang yang sama. Mengingat bahwa rata-rata manusia melepaskan sekitar 1,5 juta sel kulit per jam, membawa serta sekitar 15 juta sel bakteri, manusia jelas berkontribusi secara substansial, dan mungkin sebagian besar, keanekaragaman mikroba dalam ruangan.
Transfer langsung mikrobiota kulit melalui kontak permukaan juga telah terbukti memiliki dampak yang cukup besar dan spesifik area. Tergantung pada permukaannya, kontak kulit dapat mentransfer jutaan sel mikroba di setiap kejadian , yang mengarah pada inokulasi dan inokulasi ulang yang cepat dan terus-menerus pada permukaan yang disentuh berulang kali, seperti sakelar lampu, gagang pintu, keyboard, dispenser sabun, dan toilet. kursi . Selain itu, sejumlah penelitian telah menunjukkan bahwa mikrobiota dominan yang terkait dengan kulit manusia berbeda secara dramatis di antara individu]. Memang, dimungkinkan untuk mengidentifikasi orang berdasarkan tanda tangan mikroba unik yang mereka tinggalkan di sebuah ruangan atau di permukaan, yang memiliki aplikasi potensial yang signifikan dalam forensik. Gambar 1 menggambarkan berbagai sumber dan rute transmisi komunitas mikroba hipotetis BE dan menunjukkan bagaimana mereka dapat berkontribusi pada ekologi mikroba permukaan dalam ruangan.
Terlepas dari bukti yang menunjukkan bahwa manusia berinteraksi secara mikroba dengan ruang dalam ruangan mereka, hubungan mekanistik yang memungkinkan interaksi ini tetap dicirikan dengan buruk. Karena BE juga dapat menjadi sumber mikroba yang menjajah manusia, penting bagi kita untuk menyelidiki ‘siapa yang tinggal di mana’ di BE. Sejauh ini, literatur terutama mengeksplorasi fenomena kontaminasi jamur pada permukaan lembab ; peran kebersihan dalam menghilangkan komunitas mikroba ; dan lamanya waktu mikroba dapat bertahan hidup di permukaan. Keragaman mikroba debu juga telah dieksplorasi, seperti halnya keragaman udara dalam ruangan. Satu studi menyelidiki suksesi temporal komunitas mikroba yang dilakukan pada debu dalam ruangan dan menemukan pola musiman khusus bangunan yang merupakan kombinasi sel-sel kulit yang terlepas dari penghuni di dalam bangunan dan mikrobiota yang ditentukan secara musiman dari lingkungan eksternal.
Selain kulit manusia, aspek lain dari mikrobioma manusia juga dapat berkontribusi secara signifikan terhadap mikrobioma BE, meskipun kontribusinya cenderung lebih spesifik situasi. Seperti yang diharapkan, usus manusia dan flora vagina memainkan peran utama dalam membentuk komunitas mikroba yang terkait dengan permukaan di toilet, pusat penitipan anak dan unit perawatan intensif neonatal. Meskipun beberapa studi molekuler secara langsung menyelidiki dampak hewan peliharaan, diharapkan kulit hewan, rambut, bahan tinja (misalnya, kotoran kucing), air liur, dan kemungkinan kutu semuanya berkontribusi secara signifikan terhadap komunitas mikroba yang terkait dengan permukaan dalam ruangan dan udara . Dampak tangki ikan pada mikrobioma BE mungkin juga layak dipertimbangkan karena lingkungan ini memiliki konsorsium mikroba yang unik. Memahami kontribusi hewan penghuni mungkin sangat membantu dalam memahami penyebab asma masa kanak-kanak .
Sebagian besar pengaturan dalam ruangan juga mendapatkan sebagian besar mikrobiota mereka dari sumber lingkungan. Sampel debu di kantor secara konsisten menemukan bakteri yang berasosiasi dengan tanah dan rizosfer tanaman . Jumlah dan jenisnya tampaknya bergantung pada tingkat ventilasi luar ruangan dan iklim setempat. Kembel dan rekan menemukan perbedaan yang signifikan dalam kontribusi bakteri lingkungan alami dalam bangunan yang berventilasi baik dibandingkan dengan jendela tertutup . Rintala dan rekan kerja menunjukkan perubahan dramatis dalam mikroflora debu menurut musim yang berbeda, sementara Hewitt dan rekan menemukan sinyal iklim yang kuat di debu kantor bangunan di Tucson, Arizona (bakteri tanah gurun), dibandingkan dengan debu di New York dan San Francisco. Studi kamar kecil Flores et al . juga menemukan bakteri tanah di atas lantai kamar kecil yang mungkin berpindah dari sepatu .
Jelas, komunitas mikroba BE terdiri dari mikroba dari beragam habitat manusia dan lingkungan. Kemampuan untuk membandingkan kumpulan data metagenomik yang luas dari sekuens ribosom atau seluruh fragmen genom mikroba dari BE sink dengan komunitas sumber lingkungan, hewan dan manusia, dan penerapan alat bioinformatika yang memperkirakan kontribusi relatif dari berbagai sumber ke komunitas (misalnya, SourceTracker), akan berperan dalam memahami kolonisasi mikroba dan transmisi di BE.
Mikroba Usus Mungkin Menjadi Kunci untuk Mengatasi Alergi Makanan
Mikroba Usus Mungkin Menjadi Kunci untuk Mengatasi Alergi Makanan – Terapi baru sedang menguji apakah bakteri pelindung dapat meredam respons imun yang berbahaya terhadap makanan.
Mikroba Usus Mungkin Menjadi Kunci untuk Mengatasi Alergi Makanan
Baca Juga : Memanipulasi Ekosistem Mikroba yang Tak Terlihat Masa Depan Rumah Sakit?
hospitalmicrobiome – Sebagai seorang anak, Cathryn Nagler mengalami gatal-gatal ketika dia makan telur. Dia bereaksi terhadap penisilin. Bekerja di laboratorium setelah kuliah, dia mengembangkan alergi parah pada tikus yang menyebabkan mengi, bengkak, dan kesulitan bernapas dua kali membawanya ke ruang gawat darurat.
Saat ini, Nagler adalah seorang ahli imunologi di University of Chicago dan membantu merintis bidang penelitian yang sedang berkembang: mempelajari bagaimana bakteri dalam usus dapat dimanfaatkan untuk membantu orang dengan alergi makanan.
Bukan pengalaman pribadi dengan alergi yang mengilhami minatnya. Sebaliknya, itu adalah pengamatan aneh yang dia buat sebagai mahasiswa doktoral pada 1980-an. Dia sedang mempelajari tikus yang sistem kekebalannya rusak dan menyerang protein kolagen di dalam persendian mereka, menyebabkan radang sendi parah. Para ilmuwan dapat memulai penyakit ini dengan memberikan suntikan kolagen di bawah kulit. Tapi, anehnya, ketika Nagler kemudian memberi makan kolagen makhluk itu menggunakan tabung yang meliuk ke perut mereka, efeknya sebaliknya: Tikus menjadi lebih baik.
Beberapa dekade kemudian, konsep ini, yang disebut imunoterapi oral, telah digunakan sebagai pengobatan untuk alergi makanan, yang mempengaruhi sekitar 32 juta orang di Amerika Serikat, termasuk sekitar dua anak sekolah per kelas. Selama sepuluh tahun terakhir atau lebih, beberapa ahli alergi telah mulai merawat pasien alergi makanan dengan dosis kecil dan teratur dari makanan yang mengganggu (atau produk yang dibuat darinya) untuk menenangkan respons alergi. Pendekatan ini semakin populer dengan persetujuan pada bulan Januari dari versi standar satu set kapsul harian untuk mengobati alergi kacang oleh US Food and Drug Administration .
Tetapi imunoterapi oral memiliki kelemahan. Regimen ini bisa menegangkan, karena melibatkan konsumsi makanan sehari-hari yang bisa membunuh. Ini tidak bekerja untuk semua orang dan tidak banyak membantu memperbaiki penyakit yang mendasarinya. Sukses sebagian besar berarti memperoleh kemampuan untuk makan beberapa kacang dengan aman, misalnya, daripada bereaksi terhadap setitik tepung kacang.
Bagi beberapa keluarga, keuntungan sederhana ini mengubah hidup. Namun, itu berbahaya: Pasien harus mengonsumsi sedikit makanan setiap hari, atau beberapa kali seminggu, selama sisa hidup mereka atau mereka bisa kehilangan perlindungan .
Jadi Nagler dan beberapa peneliti lainnya sedang berupaya menemukan cara untuk mengobati alergi makanan dengan lebih mudah dan tahan lama. Mereka menargetkan apa yang mereka yakini sebagai akar penyebab ketidakseimbangan dalam komunitas bakteri menguntungkan, atau mikrobioma, yang hidup di usus kita dengan harapan mengatur ulang sistem kekebalan.
Memproduksi perawatan berbasis mikrobioma akan menjadi tantangan , dengan banyak detail yang harus dijelaskan, seperti mikroba mana yang harus disediakan dan cara terbaik untuk mengirimkannya. Tapi pendekatan ini mendapatkan momentum. Tahun lalu, tim Nagler dan kelompok lain di Boston melaporkan langkah maju yang penting: Mereka mencegah respons alergi parah pada tikus yang rentan alergi dengan memasok mikroba usus dari bayi manusia yang sehat dan tidak alergi. “Datanya bagus, dan sangat menggembirakan,” kata ahli alergi anak Jaclyn Bjelac dari Klinik Cleveland.
Dan pada bulan Maret, para ilmuwan melaporkan menemukan sejumlah besar antibodi terhadap alergen kacang di perut dan usus pasien alergi, lebih lanjut mendukung gagasan bahwa saluran pencernaan adalah hotspot untuk pengaturan dan pengobatan alergi makanan. Sudah, perusahaan sedang menguji beberapa strategi.
Sudah lama menjadi teka-teki mengapa satu orang mentolerir makanan sementara yang lain alergi tetapi, seperti yang diuraikan dalam artikel yang dia tulis bersama di Tinjauan Tahunan Imunologi , Nagler yakin bahwa mikrobioma adalah kuncinya.
Empat tahun setelah menyelesaikan pekerjaan pascasarjananya, Nagler mulai menjalankan laboratorium di Harvard Medical School. Dia sedang mempelajari penyakit radang usus, bukan alergi makanan, saat itu. Tetapi karena penelitian pada 1990-an menunjukkan bahwa penyakit radang usus terutama disebabkan oleh reaksi kekebalan terhadap bakteri usus, dia mengalihkan perhatiannya ke mikrobioma.
Kemudian, pada tahun 2000, ia menemukan publikasi yang menarik. Ini menggambarkan model tikus untuk alergi kacang yang meniru gejala utama yang dialami orang. Tikus menggaruk tanpa henti. Mata dan mulut mereka bengkak. Beberapa orang kesulitan bernapas—respons alergi yang mengancam jiwa yang disebut anafilaksis.
Semua ini terjadi setelah peneliti memberi makan tikus bubuk kacang. “Itu menarik perhatian saya,” kata Nagler. Ini bertentangan dengan temuan sebelumnya dengan tikus rematik, di mana memberi makan kolagen menenangkan reaksi kekebalan. Mengapa perbedaan?
Tikus alergi kacang, laporan lain menunjukkan, memiliki kesalahan genetik yang merusak reseptor yang disebut TLR4 yang berada di membran sel kekebalan dan mengenali mikroba. Tampaknya tikus yang alergi kacang tidak memiliki percakapan silang normal yang terjadi antara mikroba usus dan sel kekebalan.
“Itu adalah momen bola lampu saya,” kata Nagler. Mungkin triliunan mikroba yang hidup di dalam kita menekan respons imun terhadap makanan dengan merangsang reseptor TLR4. Dan mungkin gangguan dalam mikrobioma yang padat itu mengubah penekanan dan menyebabkan peningkatan alergi .
Idenya menyatu dengan tren sejarah. Seiring modernisasi masyarakat, orang-orang pindah ke daerah perkotaan, melahirkan lebih banyak bayi melalui operasi caesar, mengonsumsi lebih banyak antibiotik dan makan lebih banyak makanan olahan dan rendah serat—semuanya mengguncang mikrobioma. Waktu perubahan gaya hidup ini sejajar dengan peningkatan yang diamati dalam makanan dan jenis alergi lainnya, yang kenaikan tajamnya selama satu generasi menunjukkan beberapa penyebab lingkungan.
Pada tahun 2004, Nagler dan rekan kerjanya menerbitkan sebuah laporan yang menunjukkan bahwa kacang tanah memicu anafilaksis hanya pada tikus dengan reseptor TLR4 yang bermutasi , bukan pada galur yang terkait secara genetik dengan TLR4 normal. Perbedaannya hilang ketika para ilmuwan memusnahkan populasi bakteri usus dengan antibiotik. Kemudian, bahkan tikus normal pun menjadi rentan terhadap alergi makanan, yang menyiratkan bahwa bakteri berada di jantung perlindungan. Laboratorium Nagler telah bekerja sejak itu untuk mengidentifikasi bakteri mana yang membantu, dan untuk memahami bagaimana mereka mengatur respons alergi.
Dalam pekerjaan mereka, tim Nagler berfokus pada Clostridia dan Bacteroides dua kelompok utama bakteri dalam usus manusia. Bekerja dengan tikus yang dibiakkan di lingkungan bebas kuman dan dengan demikian tanpa mikrobioma sama sekali, tim menemukan bahwa Clostridia , tetapi bukan Bacteroides , mencegah respons alergi makanan ketika dimasukkan ke dalam usus tikus yang bersih dan berderit.
Ada penjelasan potensial: Tikus yang dijajah dengan bakteri Clostridia memiliki lebih banyak sel T pengatur, sejenis sel yang meredam respons imun. Tikus Clostridia juga menghasilkan lebih banyak molekul yang disebut IL-22 yang memperkuat lapisan usus. Sebuah teori baru mulai muncul: Jika mikroba pelindung hilang, penghalang usus melemah, memungkinkan protein makanan meresap ke dalam aliran darah dan berpotensi memicu respons alergi.
Alasan ini cocok dengan pengamatan aneh bahwa alergen makanan teratas (protein tertentu yang ditemukan dalam susu, telur, kacang tanah, kacang pohon, kedelai, gandum, ikan, dan kerang) memiliki sedikit kemiripan biokimia satu sama lain. Kesamaan mereka adalah kemampuan untuk tetap utuh di saluran pencernaan, yang biasanya memecah makanan menjadi potongan-potongan kecil yang diserap tubuh sebagai nutrisi. “Sepertinya itulah yang membuat kacang menjadi juara—kemampuannya untuk menahan degradasi di usus,” kata Nagler.
Studi lebih lanjut memperkuat hubungan antara bakteri usus dan alergi makanan dan menunjukkan bahwa dampak mikrobioma datang lebih awal dalam kehidupan. Menganalisis kotoran bayi yang sehat dan mereka yang alergi telur atau susu , para peneliti menunjukkan bahwa bayi yang alergi dan tidak alergi memiliki komunitas bakteri usus yang berbeda.
Studi lain melacak 226 anak-anak dengan alergi susu dari bayi hingga usia 8 tahun. Para ilmuwan menemukan bahwa bakteri tertentu, termasuk Clostridia , diperkaya dalam sampel tinja dari bayi berusia 3 hingga 6 bulan yang akhirnya mengatasi alergi mereka , dibandingkan dengan mereka yang tetap alergi. alergi. Para ilmuwan tidak melihat perbedaan yang sama antara kelompok-kelompok ini pada bayi yang lebih tua, menunjukkan bahwa mikroba pelindung alergi hanya dapat bertindak di awal kehidupan.
“Semua ini menunjuk pada konsep jendela peluang dalam hal pencegahan,” kata pemimpin studi Supinda Bunyavanich, ahli alergi anak di Icahn School of Medicine di Mount Sinai di New York City.
Sejak lahir, sistem kekebalan kita dididik dalam pilihan hidup atau mati. Mereka belajar membunuh kuman, tumor, dan sel-sel yang sekarat. Banyak hal lain di sekitar mereka yang harus mereka pelajari untuk tidak dibiarkan sendiri serat saraf, jaringan tulang, protein dari susu, dan kue kering yang dikonsumsi pada waktu kudapan. Studi tikus yang diterbitkan pada tahun 2019 oleh lab Nagler dan tim lain berpendapat dengan meyakinkan bahwa mikroba usus memupuk pengambilan keputusan kekebalan yang kritis ini.
Dalam salah satu penelitian, Nagler dan rekan kerjanya mengumpulkan bakteri usus dari kotoran bayi yang sehat dan alergi susu dan memasukkan kumpulan mikroba tersebut ke dalam saluran pencernaan tikus yang bebas kuman. Mereka menemukan bahwa bakteri usus dari bayi yang sehat melindungi tikus dari respons alergi terhadap susu, sedangkan mikroba dari bayi yang alergi tidak.
Menggunakan teknik matematika dan ilmu komputer untuk menganalisis hasil, tim mengidentifikasi strain bakteri yang ada pada bayi yang sehat tetapi tidak alergi. Mereka juga memeriksa aktivitas gen dalam sel-sel yang melapisi usus pola gen tertentu merupakan karakteristik dari penghalang usus yang sehat dan mencari mikroba yang keberadaannya berkorelasi dengan penghalang yang sehat.
Satu spesies Clostridia , Anaerostipes caccae , muncul dari kedua analisis. Ketika para ilmuwan mentransfer A. caccae sendirian ke tikus bebas kuman, tampaknya meniru perlindungan yang diberikan oleh mikrobioma yang sehat dan penuh.
Tim lain, yang dipimpin oleh Rima Rachid dan Talal Chatila di Boston Children’s Hospital, mengambil pendekatan serupa menggunakan tikus hiper-alergi, menemukan bahwa spesies tunggal Subdoligranulum variabile dan satu set spesies Clostridia mencegah respons alergi . Sel T pengatur adalah kunci untuk respons dan didorong untuk bertindak oleh mikroba.
Studi ini dan lainnya dengan jelas menunjukkan bahwa mikrobioma penting untuk mencegah alergi makanan dan mendorong toleransi, kata Carina Venter, ahli diet penelitian di University of Colorado di Denver yang mempelajari hubungan antara diet ibu selama kehamilan, mikrobioma bayi dan risiko eksim. dan alergi. Tapi, katanya, “bagaimana mikrobioma itu harus terlihat dalam hal keragaman dan dalam hal strain tertentu, kita tidak tahu.”
Banyak hal yang tidak diketahui meninggalkan kebingungan bagi para peneliti yang berharap untuk mengembangkan pengobatan yang lebih baik untuk alergi makanan: Apakah lebih baik untuk menyediakan mikrobioma yang sehat dan lengkap, atau untuk mengisi hanya beberapa mikroba yang berguna? “Saya menggaruk-garuk kepala setiap hari memikirkan hal ini,” kata Rachid.
Dia memimpin studi klinis untuk menguji kemungkinan pertama. Dalam uji coba kecil ini , orang dewasa dengan alergi kacang akan menelan pil yang mengandung bakteri usus dari donor sehat yang telah disaring sebelumnya untuk keamanan oleh bank tinja nirlaba OpenBiome. Pendekatan, yang dikenal sebagai transplantasi tinja , tidak disetujui FDA tetapi semakin banyak digunakan untuk mengobati gangguan usus yang parah dengan tujuan memperbaiki mikrobioma yang sakit dengan memasukkan mikrobioma yang sehat dan seimbang.
Uji coba lain juga sedang berlangsung. Menggunakan strain pelindung yang diidentifikasi oleh tim Boston, Pareto Bio dari La Jolla, California, sedang mengembangkan produk mikroba hidup untuk mengobati alergi makanan. Perusahaan lain, Vedanta Biosciences of Cambridge, Massachusetts, sedang mengembangkan kapsul probiotik yang mengandung campuran strain Clostridia yang dipilih karena kemampuannya untuk menginduksi sel T regulator . Vedanta sedang menguji kapsul sebagai tambahan untuk imunoterapi oral pada orang dewasa dengan alergi kacang.
Perusahaan ketiga, Prota Therapeutics of Melbourne, Australia, mengkomersialkan strategi serupa yang menggabungkan imunoterapi oral kacang dengan probiotik dalam kasus mereka, galur Lactobacillus yang biasa diresepkan untuk masalah pencernaan.
Mengelola seluruh mikrobioma dari donor bukan tanpa risiko: Empat pasien telah dirawat di rumah sakit, dan satu meninggal, akibat infeksi serius yang terkait dengan transplantasi tinja . Jadi beberapa peneliti berpikir mungkin lebih baik menggunakan spesies yang ditentukan secara tepat. Meskipun risiko ini melemahkan manfaat, “Anda cenderung tidak menyebabkan masalah yang tidak terduga,” kata Wayne Shreffler, yang memimpin pusat alergi makanan di Rumah Sakit Umum Massachusetts di Boston dan memimpin studi Vedanta.
Memanipulasi Ekosistem Mikroba yang Tak Terlihat Masa Depan Rumah Sakit?
Memanipulasi Ekosistem Mikroba yang Tak Terlihat Masa Depan Rumah Sakit? – Ketika berbicara tentang mikroba, para ahli biasanya memfokuskan desain dan perilaku rumah sakit untuk meminimalkan penyebaran patogen tertentu. Tetapi bidang penelitian yang muncul melihat seluruh mikrobioma yang dibangun.
Memanipulasi Ekosistem Mikroba yang Tak Terlihat Masa Depan Rumah Sakit?
Baca Juga : Kehidupan Ekologi Mikroba Yang Sangat Beragam
hospitalmicrobiome – Kamar rumah sakit mungkin terasa steril, dengan udara daur ulang dan permukaan halus yang digosok. Tapi di balik selubung antiseptik itu ada dunia mikroba yang tak terlihat, yang komposisinya terus berubah.
Setiap pasien baru membawa mikrobioma mereka sendiri kumpulan bakteri dan mikroba lain yang hidup di dalam dan di tubuh yang mereka tumpahkan di ranjang rumah sakit, remote televisi, dan apa pun yang mereka sentuh. Setiap perawat, dokter, dan pengunjung yang memasuki ruangan juga meneteskan mikroba. Organisme kecil juga bersirkulasi melalui sistem ventilasi dan bergerak melalui udara. Beberapa tidak berasal dari manusia tetapi sistem air, pemanas, dan lingkungan khusus buatan manusia lainnya. Secara kolektif, mikroba ini membentuk mikrobioma yang dibangun, yang ada dalam bentuk yang unik dan dinamis di setiap bangunan di planet ini.
Tidak semua mikroba itu buruk, tentu saja. Sebagian besar jinak atau bahkan bermanfaat. Tetapi agen penyebab penyakit selalu ada di rumah sakit, dan setiap hari satu dari 25 pasien mendapat setidaknya satu infeksi yang tidak disengaja selama mereka tinggal di rumah sakit.
Beberapa peneliti menduga bahwa ekosistem mikroba rumah sakit dapat mempengaruhi penyebaran patogen, yang pada gilirannya dapat mempengaruhi kesehatan manusia. Meskipun penelitian ini masih dalam tahap awal, ini dapat menyebabkan perubahan dalam desain atau praktik rumah sakit untuk mempromosikan mikrobioma yang dibangun lebih sehat.
Memperluas Fokus
Para peneliti telah tertarik pada mikroba di rumah sakit setidaknya sejak tahun 1847, ketika Ignaz Semmelweis, seorang dokter Jerman-Hongaria, menemukan bahwa mahasiswa kedokteran di sebuah rumah sakit Wina secara tidak sengaja menularkan sepsis nifas dari ruang otopsi ke bangsal bersalin, yang menyebabkan tingkat kematian yang tinggi. Semmelweis memperkenalkan cuci tangan wajib, intervensi pertama untuk infeksi yang didapat di rumah sakit dalam catatan.
Sejak itu, sebagian besar penelitian mikroba di rumah sakit juga berfokus pada pencegahan wabah patogen tertentu, terutama yang berbahaya bagi orang yang sudah sakit atau memiliki sistem kekebalan yang lemah. Pada tahun 1976, misalnya, para ilmuwan pertama kali menemukan bakteri yang menyebabkan Penyakit Legiuner, Legionella pneumophila , setelah wabah di konvensi American Legion di Philadelphia. Bakteri, yang dapat menyebabkan pneumonia fatal, hidup di menara pendingin sebuah hotel dan beredar melalui AC gedung.
Patogen juga dapat berkembang biak di air mancur minum dan pemanas air panas, dan merupakan perhatian khusus dalam sistem air rumah sakit. Sejak penemuannya, wabah telah diidentifikasi di rumah sakit di seluruh dunia. Untuk mencegah bakteri bertahan dan menyebar dari sumbernya ke kamar pasien, rumah sakit secara teratur membersihkan dan memelihara sistem ventilasi dan menempatkan menara pendingin sehingga udara yang berpotensi terinfeksi tidak dapat bersirkulasi.
“Beberapa orang sekarang mencoba memahami seluruh ekosistem, bukan hanya dampak patogen.”
Saat ini, contoh lain dari patogen rumah sakit termasuk jamur hitam dari genus Stachybotrys , yang dapat memicu penyakit pernapasan dan dapat dikendalikan dengan sistem sanitasi ultraviolet, dan bakteri Clostridium difficile , yang menyebabkan gangguan pencernaan yang parah dan dapat dihilangkan dari ruangan yang terkontaminasi oleh robot. memuntahkan uap hidrogen peroksida. Bakteri resisten antibiotik seperti Staphylococcus aureus yang resisten methicillin (MRSA), yang dapat menyebabkan infeksi yang tidak dapat diobati, dapat dilacak dengan teknik pengurutan genom. Menemukan sumber bakteri dengan peta genetik untuk melihat bagaimana mereka bermutasi dari waktu ke waktu dapat mendorong perubahan perilaku staf rumah sakit, seperti lebih berhati-hati untuk mencuci tangan dan mengkarantina pasien yang terinfeksi.
Tetapi bakteri dan jamur ini tidak hidup dalam ruang hampa. Mereka berinteraksi dengan mikroba lain seperti seorang pembunuh mungkin memiliki jaringan rekan konspirator dan pengamat yang membantu atau menghalangi tindakan mereka. Memahami hubungan ini dapat membantu menjelaskan keberhasilan atau kegagalan patogen.
“Apa yang baru—dan sangat penting dan menarik—adalah bahwa beberapa orang mencoba memahami seluruh ekosistem, bukan hanya dampak patogen,” jelas Jonathan Eisen, ahli biologi evolusi di University of California, Davis yang berspesialisasi dalam mikroba. di lingkungan binaan. “Jika kita ingin memahami mengapa MRSA menyebar di rumah sakit, kita mungkin harus memahami seluruh kumpulan mikroba di rumah sakit.”
Langkah Awal
Laboratorium Eisen mengawasi Microbiology of the Built Environment Network (microBEnet), sumber online yang melacak sekitar dua lusin kelompok yang bekerja untuk memahami mikroba tidak hanya di rumah sakit, tetapi juga di lingkungan binaan lainnya termasuk berbagai bangunan, mobil, dan pesawat terbang.
Meskipun kita menghabiskan sekitar 90 persen waktu kita di dalam ruangan, mikrobioma lingkungan buatan adalah salah satu yang terakhir dieksplorasi para ilmuwan. Seperti pekerjaan lain yang pernah dilakukan sebelumnya termasuk penelitian mikroba di laut, tanah, dan bahkan manusia Eisen dan rekan-rekannya telah mendapat manfaat dari kemajuan teknologi pengurutan genom, yang dapat mengidentifikasi kode genetik organisme dengan relatif cepat dan murah. Menyeka ruangan dan kemudian menjalankan sampel melalui mesin pengurutan dapat mengidentifikasi mikroba, dan melacak dari mana penyeka berasal dapat menunjukkan di mana mereka tinggal.
Sistem ventilasi yang berbeda dapat mempengaruhi kandungan mikroba ruangan.
Beberapa peneliti sudah menggunakan teknik ini untuk mengeksplorasi mikrobioma rumah sakit. Pada tahun 2012, para peneliti di Pusat Biologi dan Lingkungan Buatan (BioBE) di Universitas Oregon menerbitkan sebuah makalah yang melihat kandungan mikroba di udara di Rumah Sakit Providence Milwaukie di Oregon. Para peneliti mengambil sampel udara dari kamar rumah sakit yang berventilasi baik dengan jendela terbuka atau sistem mekanis dan menemukan bahwa yang pertama memiliki keragaman bakteri yang lebih besar. Tetapi ruangan yang berventilasi mekanis dan dengan demikian terkena sejumlah kecil udara luar juga memiliki lebih banyak bakteri yang terkait dengan patogen manusia. Meskipun ini tidak berarti bahwa jendela yang terbuka pasti akan bermanfaat bagi kesehatan pasien, penelitian tersebut menunjukkan bagaimana sistem ventilasi yang berbeda dapat memengaruhi kandungan mikroba ruangan.
Orang yang menghabiskan waktu di sebuah ruangan mungkin terpengaruh oleh mikrobiomanya, termasuk mikroba non-patogen. Awal tahun ini, sebuah tim yang dipimpin oleh para peneliti di University of California, Berkeley menerbitkan penelitian yang melihat hubungan antara mikroba lingkungan dan bayi di unit perawatan intensif neonatal di Magee-Womens Hospital dari University of Pittsburgh Medical Center.
Bayi biasanya dijajah dengan bakteri yang menjadi primadona mikrobioma mereka ketika mereka lahir. Tetapi bayi prematur di unit neonatal adalah kasus khusus mereka kurang berkembang dan seringkali harus diobati dengan antibiotik, yang berarti mikrobioma mereka mungkin memiliki permulaan yang lambat. Meskipun unit neonatus dijaga sesteril mungkin untuk membantu mencegah bayi jatuh sakit, para peneliti Berkeley menemukan bahwa mikroba di berbagai permukaan di unit Pittsburg sebagian besar terkait dengan kulit manusia secara genetik sangat mirip dengan yang ada di saluran pencernaan bayi. bayi prematur yang tinggal di unit selama bulan pertama kehidupan mereka. Mikroba lingkungan kemungkinan besar menjajah bayi, sama seperti mikroba ibu biasanya akan menyusup ke tubuh mereka selama kelahiran.
Pemindaian serupa di kamar rumah sakit lain, dari tempat pasien tidur hingga tempat mereka dirawat, dapat mengungkapkan cara serupa bahwa orang dan lingkungan binaan bertukar mikroba.
Sampel Besar
Proyek yang lebih besar sedang dalam perjalanan. Proyek Mikrobioma Rumah Sakit , misalnya, baru-baru ini menyelesaikan data selama satu tahun di Pusat Perawatan dan Penemuan, sebuah rumah sakit baru yang terkait dengan Universitas Chicago. Sampel dikumpulkan setiap hari di sepuluh ruangan yang hampir identik dalam hal tata letak dan ventilasi.
“Ini adalah 15.000 sampel dalam satu lingkungan dengan resolusi harian dalam setahun,” kata Jack Gilbert, ahli ekologi mikroba di University of Chicago dan salah satu pemimpin proyek, “Ini akan menjadi salah satu lingkungan yang paling bercirikan mikroba di Bumi.”
Tim Gilbert dapat memulai pengumpulan data setelah rumah sakit dibangun tetapi sebelum pasien tiba, untuk melihat bagaimana orang-orang mengubah lingkungan. Kelompok ini juga bekerja dengan ilmuwan bangunan termasuk Brent Stephens dari Institut Teknologi Illinois, yang mengkarakterisasi fitur utama bangunan dan merancang cara untuk mengumpulkan berbagai data lingkungan yang mungkin berperan dalam kehidupan mikroba.
“Apa yang perlu kita ketahui tentang bangunan yang kita sampel dari perspektif mikroba? Ada banyak bukti yang menunjukkan manusia adalah sumber bakteri yang sangat besar, dan banyak di antaranya yang cukup baru, ”kata Stephens. “Jadi mungkin jumlah orang di lingkungan ini penting. Dan sejauh bertahan hidup di permukaan, kita tahu bahwa suhu dan kelembaban memiliki pengaruh besar pada komunitas mikroba.”
Untuk mengumpulkan semua informasi itu, tim Stephens menempatkan beberapa jenis data logger di setiap ruang belajar untuk mengukur suhu, kelembaban, tekanan, dan cahaya. Mereka juga menambahkan sensor inframerah ke setiap pintu yang, bersama dengan sensor karbon dioksida, dapat memperkirakan bagaimana orang yang berbeda memasuki ruangan setiap hari.
Hasil awal menunjukkan peningkatan besar dalam keragaman mikroba setelah rumah sakit mulai menerima pasien. Digabungkan dengan informasi genetik yang akan mengidentifikasi spesies bakteri tertentu dan lokasinya, data lingkungan dapat mengungkapkan bagaimana faktor-faktor ini memengaruhi keberadaan dan pertumbuhan mikroba.
Meskipun sebuah makalah tentang penelitian ini kemungkinan tidak akan diterbitkan hingga setidaknya tahun 2015, Gilbert mengatakan hasil awal menunjukkan peningkatan besar dalam keragaman mikroba setelah rumah sakit mulai menerima pasien, yang tidak mengherankan. Hasil awal juga menunjukkan bahwa mikroba di kamar rumah sakit mungkin tidak hanya bergantung pada berapa lama pasien tinggal di kamar, tetapi juga pada perawatan apa yang diterima pasien—bagaimana mereka diobati dengan antibiotik, misalnya, atau apakah mereka menjalani kemoterapi. Ekosistem mikroba yang berbeda ini dapat mempengaruhi bagaimana infeksi yang didapat di rumah sakit menyebar.
“Kami berpikir bahwa komunitas mikroba lainnya di rumah sakit berdampak pada bagaimana patogen dipindahkan dengan cara yang sama seperti ketika patogen yang menemukan jalannya ke sungai tiba-tiba menemukan dirinya dikelilingi oleh bakteri tanah dan sering kali kalah bersaing dan tidak dapat bertahan hidup, kata Gilbert. “Kami pikir hal yang sama terjadi di lingkungan rumah sakit. Jika ada mikroflora yang kaya, patogen tidak dapat bersaing. Tetapi jika mikroflora itu tidak ada karena sterilisasi fasilitas, misalnya, ia dapat bertahan lebih lama.”
Maka, mungkin saja ruangan yang kurang steril dapat mengurangi prevalensi mikroba berbahaya. “Lebih banyak pekerjaan harus dilakukan untuk memvalidasi hipotesis, tetapi setidaknya sekarang kita memiliki konteks rumah sakit yang sangat kaya,” kata Gilbert.
Masa Depan Desain Rumah Sakit?
Tentu saja, beberapa bagian rumah sakit akan selalu membutuhkan sterilisasi yang cermat, seperti ruang operasi. Dan secara umum, pengendalian infeksi merupakan tujuan utama di setiap rumah sakit. “Kami mencoba membunuh semua patogen,” kata Nancy Iversen, Direktur Keselamatan Pasien dan Pengendalian Infeksi di Klinik Billings di Montana. “Itulah yang kami kejar di rumah sakit, kami mencoba membunuh mereka semua dan menjauhkan mikroorganisme dari udara dan menyediakan lingkungan yang terlindungi bagi pasien kami yang berisiko, sebagian besar karena wabah.”
Sementara Iverson tertarik dengan implikasi dari mikrobioma yang dibangun dan peran bakteri menguntungkan, dia khawatir tentang keselamatan pasien. Selain itu, ia menambahkan, ada banyak hambatan potensial yang melibatkan pedoman peraturan: “Bagaimana Anda membuat pasien mendaftar dalam studi di mana Anda tidak mendisinfeksi secara tradisional di bawah standar regulator apa yang dibutuhkan oleh Pusat Pengendalian Penyakit, apa yang dibutuhkan oleh badan-badan lain ini mengenai tindakan yang Anda ambil selama konstruksi dan pembersihan serta aliran udara?”.
Namun, penelitian tentang mikrobioma yang dibangun sudah mempengaruhi bagaimana beberapa arsitek berpikir tentang desain bangunan. “Lensa yang saya gunakan dalam melihat bangunan telah memperoleh dimensi baru sejak menjadi bagian dari penelitian ini,” kata Jeff Kline, peneliti arsitektur dan ilmuwan bangunan di BioBE Center di University of Oregon. “Sekarang saya mengerti, setidaknya sedikit, tentang bagaimana keputusan arsitektur tentang bentuk bangunan, organisasi, bahan, dan sistem, terutama ventilasi, menyediakan mekanisme yang memengaruhi komposisi mikrobioma dalam ruangan.”
Kehidupan Ekologi Mikroba Yang Sangat Beragam
Kehidupan Ekologi Mikroba Yang Sangat Beragam – Kehidupan mikroba sangat beragam dan mikroorganisme secara harfiah menutupi planet ini. Faktanya, telah diperkirakan bahwa ada 100.000.000 kali lebih banyak sel mikroba di planet ini daripada jumlah bintang di alam semesta yang dapat diamati! Mikroba hidup di semua bagian biosfer di mana terdapat air cair, termasuk tanah, mata air panas, dasar laut, danau asam, gurun, geyser, batu, dan bahkan usus mamalia.
Kehidupan Ekologi Mikroba Yang Sangat Beragam
hospitalmicrobiome – Berdasarkan kemahahadirannya, mikroba berdampak pada seluruh biosfer memang, proses metabolisme mikroba (termasuk fiksasi nitrogen, metabolisme metana, dan metabolisme belerang) secara kolektif mengontrol siklus biogeokimia global. Kemampuan mikroba untuk berkontribusi secara substansial terhadap fungsi setiap ekosistem merupakan cerminan keanekaragaman hayati yang luar biasa.
Mikroba sangat penting untuk setiap ekosistem di Bumi dan sangat penting di zona di mana cahaya tidak dapat mendekat (yaitu, di mana fotosintesis tidak dapat menjadi sarana dasar untuk mengumpulkan energi). Mikroorganisme berpartisipasi dalam sejumlah proses ekologi mendasar termasuk produksi, dekomposisi, dan fiksasi. Mereka juga dapat memiliki efek tidak langsung tambahan pada ekosistem melalui hubungan simbiosis dengan organisme lain. Selain itu, proses mikroba dapat dikooptasi untuk biodegradasi atau bioremediasi limbah domestik, pertanian, dan industri, membuat studi ekologi mikroba sangat penting untuk aplikasi bioteknologi dan lingkungan.
Setiap spesies dalam suatu ekosistem dianggap menempati ceruk unik yang terpisah. Relung ekologi suatu mikroorganisme menggambarkan bagaimana ia menanggapi distribusi sumber daya dan spesies yang bersaing, serta cara-cara di mana ia mengubah faktor-faktor yang sama pada gilirannya. Intinya, ceruk adalah deskripsi kompleks tentang cara spesies mikroba menggunakan lingkungannya.
Relung ekologi yang tepat dari suatu mikroba terutama ditentukan oleh sifat metabolisme spesifik organisme itu. Misalnya, organisme mikroba yang dapat memperoleh energi dari oksidasi senyawa anorganik (seperti bakteri pereduksi besi ) kemungkinan akan menempati relung yang berbeda dari organisme yang memperoleh energi dari cahaya (seperti cyanobacteria). Bahkan di antara bakteri fotosintetik, ada berbagai spesies yang mengandung pigmen fotosintetik yang berbeda (seperti klorofil dan karotenoid) yang memungkinkan mereka memanfaatkan bagian spektrum elektromagnetik yang berbeda oleh karena itu, bahkan mikroba dengan sifat metabolik yang sama dapat menghuni relung yang unik.
Baca Juga : Analisis Mikroorganisme di Lingkungan Rumah Sakit dan Potensi Risiko
Organisasi Ekosistem
Meskipun ahli ekologi cenderung menganggap ekosistem sebagai unit struktural dasar, mungkin sulit (jika bukan tidak mungkin) untuk secara formal mendefinisikan batas-batas ekosistem tertentu. Dengan demikian, ekosistem lebih baik dianggap sebagai konseptual daripada lokasi geografis yang sebenarnya. Jarang ekosistem terisolasi satu sama lain melainkan, mereka harus dianggap sebagai bagian dari keseluruhan fungsi yang lebih besar yang bersama-sama membentuk biosfer (“tempat di permukaan bumi di mana kehidupan tinggal”).
Terlepas dari kenyataan bahwa batas-batas yang jelas antara ekosistem mungkin sulit untuk diidentifikasi, berbagai interaksi yang terjadi dalam komunitas ekologi sering dapat diamati dan didefinisikan. Interaksi ini mungkin paling baik dijelaskan dengan merinci hubungan makan (apa makan apa) di antara biota dalam suatu ekosistem, sehingga menghubungkan ekosistem ke dalam sistem pertukaran terpadu.
Dalam ekosistem, faktor biotik yang terdiri dari kategori di atas dapat diatur ke dalam rantai makanan di mana produsen autotrofik menggunakan bahan dan nutrisi yang didaur ulang oleh pengurai untuk membuat makanan mereka sendiri produsen pada gilirannya dimakan oleh konsumen heterotrofik. Dalam ekosistem dunia nyata, ada beberapa rantai makanan untuk sebagian besar organisme (karena sebagian besar organisme memakan lebih dari satu jenis makanan atau dimakan oleh lebih dari satu jenis pemangsa).
Selain itu, pergerakan nutrisi mineral dalam rantai makanan bersifat siklik daripada linier. Akibatnya, jaringan rumit dari rantai makanan yang berpotongan dan tumpang tindih untuk suatu ekosistem lebih sering direpresentasikan sebagai jaring makanan. Sebuah jaring makanan menggambarkan kumpulan konsumen heterotrofik yang jaringan dan siklus aliran energi dan nutrisi dari basis produktif autotrof makan sendiri.
Selain itu, pergerakan nutrisi mineral dalam rantai makanan bersifat siklik daripada linier. Akibatnya, jaringan rumit dari rantai makanan yang berpotongan dan tumpang tindih untuk suatu ekosistem lebih sering direpresentasikan sebagai jaring makanan. Sebuah jaring makanan menggambarkan kumpulan konsumen heterotrofik yang jaringan dan siklus aliran energi dan nutrisi dari basis produktif autotrof makan sendiri.
Mikroorganisme memainkan peran penting dalam setiap komunitas ekologi dengan melayani baik sebagai produsen maupun sebagai pengurai. Meskipun tanaman adalah produsen utama yang paling umum, mikroba fotosintesis autotrofik (seperti cyanobacteria dan alga) dapat memanfaatkan energi cahaya untuk menghasilkan bahan organik.
Selain itu, di zona di mana cahaya tidak dapat menembus (dan dengan demikian fotosintesis tidak dapat menjadi sarana dasar untuk menghasilkan energi), mikroba kemosintetik menyediakan energi dan karbon untuk organisme lain dalam ekosistem. Mikroba lain adalah pengurai, dengan kemampuan untuk mendaur ulang nutrisi dari bahan organik mati dan produk limbah organisme lain.
Peran Mikroba dalam Siklus Biogeokimia
Nutrisi bergerak melalui ekosistem dalam siklus biogeokimia. Siklus biogeokimia adalah jalur di mana unsur kimia (seperti karbon atau nitrogen) bersirkulasi melalui faktor biotik (hidup) dan abiotik (tidak hidup) suatu ekosistem. Unsur-unsur yang bergerak melalui faktor-faktor ekosistem tidak hilang tetapi malah didaur ulang atau terakumulasi di tempat yang disebut reservoir (atau “tenggelam”) di mana mereka dapat ditahan untuk jangka waktu yang lama. Unsur, senyawa kimia, dan bentuk materi lainnya diteruskan dari satu organisme ke organisme lain dan dari satu bagian biosfer ke bagian lain melalui siklus biogeokimia ini.
Ekosistem memiliki banyak siklus biogeokimia yang beroperasi sebagai bagian dari sistem. Contoh yang baik dari molekul yang didaur ulang dalam suatu ekosistem adalah air, yang selalu didaur ulang melalui siklus air. Air mengalami penguapan, kondensasi, dan kemudian jatuh kembali ke Bumi sebagai hujan (atau bentuk presipitasi lainnya). Ini melambangkan siklus yang diamati untuk semua elemen utama kehidupan.
Meskipun siklus biogeokimia dalam ekosistem tertentu dikoordinasikan oleh organisme hidup yang lengkap dan faktor abiotik yang membentuk sistem itu, mikroorganisme memainkan peran utama dalam mengatur sistem biogeokimia di hampir semua lingkungan planet kita.
Ini termasuk lingkungan ekstrim seperti danau asam dan ventilasi hidrotermal, dan bahkan termasuk sistem kehidupan seperti usus manusia. Proses metabolisme kolektif utama mikroba (termasuk fiksasi nitrogen, fiksasi karbon, metabolisme metana, dan metabolisme belerang) secara efektif mengontrol siklus biogeokimia global. Luar biasa, produksi oleh mikroba begitu besar sehingga biogeokimia global kemungkinan besar tidak akan berubah bahkan jika kehidupan eukariotik sama sekali tidak ada!
Siklus Karbon
Karbon sangat penting untuk kehidupan karena merupakan blok bangunan penting dari semua senyawa organik. Tumbuhan dan hewan memanfaatkan karbon untuk menghasilkan karbohidrat, lemak, dan protein, yang kemudian dapat digunakan untuk membangun struktur internal mereka atau untuk memperoleh energi.
Karbon dalam bentuk karbon dioksida (CO 2 ) mudah diperoleh dari atmosfer, tetapi sebelum dapat dimasukkan ke dalam organisme hidup harus diubah menjadi bentuk organik yang dapat digunakan. Proses transformatif dimana karbon dioksida diambil dari reservoir atmosfer dan “difiksasi” menjadi zat organik disebut fiksasi karbon. Mungkin contoh fiksasi karbon yang paling terkenal adalah fotosintesis, sebuah proses di mana energi yang berasal dari sinar matahari dimanfaatkan untuk membentuk senyawa organik. Fotosintesis tergantung pada aktivitas mikroorganisme seperti cyanobacteria memang, fakta bahwa ada oksigen di atmosfer bumi adalah konsekuensi dari aktivitas fotosintesis mikroba purba.
Siklus Nitrogen
Nitrogen sangat penting untuk semua bentuk kehidupan karena diperlukan untuk sintesis bahan dasar kehidupan (misalnya, DNA, RNA, dan asam amino). Atmosfer bumi terutama terdiri dari nitrogen, tetapi nitrogen atmosfer (N 2 ) relatif tidak dapat digunakan untuk organisme biologis. Akibatnya, proses kimia nitrogen (atau fiksasi nitrogen) diperlukan untuk mengubah gas nitrogen menjadi bentuk yang dapat digunakan organisme hidup.
Hampir semua fiksasi nitrogen yang terjadi di planet ini dilakukan oleh bakteri yang memiliki enzim nitrogenase, yang menggabungkan N2 dengan hidrogen untuk menghasilkan bentuk nitrogen yang berguna (seperti amonia). Dengan demikian, mikroorganisme sangat penting untuk bentuk kehidupan tumbuhan dan hewan, yang tidak dapat memfiksasi nitrogen sendiri.
Analisis Mikroorganisme di Lingkungan Rumah Sakit dan Potensi Risiko
Analisis Mikroorganisme di Lingkungan Rumah Sakit dan Potensi Risiko – Laporan ini memberikan informasi tentang kualitas udara dalam ruangan dan potensi risiko terkait di rumah sakit. Penyebaran dan persistensi komunitas mikroba di lingkungan rumah sakit sangat menarik bagi kesehatan masyarakat.
Analisis Mikroorganisme di Lingkungan Rumah Sakit dan Potensi Risiko
hospitalmicrobiome – Rumah sakit dicirikan oleh risiko infeksi yang tinggi, pertama penyebab kondisi imunologis pasien yang terganggu yang membuat mereka rentan terhadap infeksi oportunistik bakteri, virus, parasitologi dan jamur. Bukti menunjukkan bahwa agen mikroba menyebar melalui udara, permukaan, aerosol dan tangan.
Jika permukaan dapat bertindak sebagai reservoir untuk beberapa patogen, tangan merupakan jalur transmisi yang penting. Mikroorganisme yang ditularkan melalui udara dan aerosol yang terbawa air dipertimbangkan, dan keberadaannya di lingkungan rumah sakit ditinjau.
Istilah lingkungan rumah sakit mencakup bangunan rumah sakit dan pengaturan perawatan kesehatan dengan semua komponen dalam ruangan yang membedakannya: menempati orang (orang sakit, pengunjung dan staf rumah sakit), udara dalam ruangan, permukaan, peralatan medis, obat-obatan, peralatan medis, makanan dan limbah (Bottero et al. .2015 ; Capolongo dkk. 2016 ).
Semua komponen ini berpotensi mendukung kelangsungan hidup dan pertumbuhan agen biologis. Bagaimana komunitas mikroba bertahan dan berubah di lingkungan dalam ruangan menjadi perhatian besar bagi kesehatan masyarakat. Faktanya, penelitian terbaru menunjukkan bahwa ketika manusia menempati suatu ruang, manusia di sana mengubah mikrobiota ruang tersebut (Smith et al. 2013 ; Capolongo et al. 2015b ).
Di dalam rumah sakit, orang dapat terpapar bioaerosol, partikel asal biologis yang tersuspensi di udara, dan potensi tertular mikroba patogen tinggi. Paparan patogen pada manusia dapat dikaitkan dengan berbagai masalah kesehatan masyarakat utama, seperti penyakit menular, efek toksik akut, dan alergi.
Lingkungan rumah sakit dicirikan oleh risiko infeksi yang tinggi, pertama karena kondisi imunologis pasien yang terganggu sehingga rentan terhadap infeksi oportunistik bakteri, virus, parasitologi dan jamur (D’Alessandro et al. 2016 ). Potensi transmisi bahan biologis selama operasi operasi dan perawatan medis dari individu yang terinfeksi membuat lingkungan rumah sakit sangat rentan terkontaminasi dengan penyebaran patogen di antara pasien (Baglioni dan Capolongo 2002 ).
Selanjutnya, dalam dekade terakhir, jika penggunaan antibiotik telah menjadi alat yang sangat baik untuk mencegah infeksi nosokomial, penggunaan obat-obatan ini secara ekstensif pasti telah menyebabkan timbulnya kejadian resistensi antibiotik.
Bangunan rumah sakit dapat dianggap sebagai lingkungan dinamis yang dipengaruhi oleh beberapa faktor yang secara aktif berkontribusi untuk menentukan risiko infeksi bagi pasien. Aspek yang harus diperhatikan diwakili oleh jumlah penghuni (selain pasien, petugas medis dan pengunjung), keadaan kesehatan mereka yang efektif, kebiasaan dan aktivitas higienis yang terjadi setiap saat di rumah sakit (Capolongo et al. 2015a ; Astley dkk.2015 ) .
Kondisi higienis situs dan ruangan, bahan bangunan dan peralatan, perabotan juga mempengaruhi komposisi komunitas mikroba (Signorelli et al. 2016). Selain itu, perangkat teknologi seperti sistem hidraulik, pemanas, dan AC dapat menjadi sumber potensial bakteri, jamur (jamur), virus, dan organisme lain jika tidak dirancang dan diserahkan ke pemeliharaan preventif yang direncanakan secara memadai.
Kondisi iklim mikro dan kejadian yang tidak disengaja dapat mendukung pertumbuhan mikroba dan jamur (infiltrasi dan kondensasi air) yang menyebabkan kondisi dalam ruangan yang berbahaya (Buffoli et al. 2007 ). Beban mikroba luar ruangan dan karakteristik iklim musiman juga mempengaruhi kualitas mikrobiologis udara dalam ruangan rumah sakit.
Sumber Infeksi yang Didapat di Rumah Sakit dan Rute Penularannya
Infeksi yang didapat di rumah sakit muncul sebagai penyebab penting morbiditas dan mortalitas pada pasien dengan gangguan sistem imun dan penyakit dasar yang parah. Setiap tahun, 2 juta pasien menderita infeksi yang didapat di rumah sakit dan hampir 100.000 di antaranya meninggal (Klevens et al. 2007 ).
Data dari Organisasi Kesehatan Dunia menunjukkan bahwa pada 100 pasien rawat inap, 7-10 diperkirakan tertular, setidaknya, satu infeksi terkait perawatan kesehatan (WHO 2011 ). Namun, beban sebenarnya tidak diketahui karena sulitnya mengumpulkan data yang dapat diandalkan. Faktanya, diagnosis infeksi nosokomial sangat kompleks dan didasarkan pada beberapa kriteria dan bukan pada satu tes laboratorium.
Di fasilitas kesehatan, sumber utama infeksi adalah pasien dan petugas kesehatan, meskipun lingkungan juga berperan penting. Faktanya, lingkungan dapat bertindak sebagai reservoir bagi mikroorganisme infektif potensial dan dapat berkontribusi pada penyebarannya. Akibatnya, bakteri juga umum pada permukaan benda mati, peralatan dan udara dalam ruangan.
Pasien yang terinfeksi menyebarkan mikroorganisme di lokasi rumah sakit melalui pelepasan tetes ekspektorat, cairan dari luka yang terinfeksi, kotoran, urin, darah, cairan tubuh lainnya, tetapi juga melalui pakaian dan selimut. Selain mikroorganisme patogen, flora endogen pasien dapat menjadi sumber mikroba yang konsisten.
Penyebaran mikroba sebagian besar terjadi melalui tetesan besar, kontak langsung dengan bahan infeksius atau melalui kontak dengan benda mati yang terkontaminasi oleh bahan infeksius. Kontak langsung antara pasien jarang terjadi; Tangan petugas klinis dapat menyebarkan mikroorganisme infektif dan merupakan sarana infeksi nosokomial yang paling sering. Dengan demikian, kebersihan tangan diakui sebagai tindakan utama untuk mengurangi infeksi.
Baca Juga : Penelitian Mikrobioma di Rumah Sakit USA
Bahkan orang dan staf yang sehat dapat bertindak sebagai pembawa ketika terinfeksi atau dijajah. Patogen seperti Staphylococcus aureus, Staphylococcus pyogenes, Neisseria meningitidis, Corynebacterium diphtheriae, virus hepatitis B, cytomegalovirus dapat ditularkan oleh pembawa tanpa gejala.
Patogen dan patogen oportunistik mungkin ada dalam sistem distribusi air dan dalam aerosol yang dilepaskan oleh sistem pendingin air (misalnya Legionella sp., Mycobacterium sp.). Kontaminasi mikroba juga dapat terjadi pada obat-obatan selama distribusi di antara pasien dan pada makanan yang diproses secara tidak benar. Selain itu, limbah rumah sakit yang tidak tepat dan cepat dibuang dapat menjadi sumber kontaminasi yang berbahaya.
Mikroorganisme yang dapat menyebar melalui kontak termasuk yang terkait dengan impetigo, abses, penyakit diare, kudis dan organisme yang resisten antibiotik (Staphylococcus aureus yang resisten methicillin dan enterococci yang resisten vankomisin). Penularan melalui vektor terbatas pada daerah di mana serangga, artropoda dan parasit tersebar luas.
Air dan larutan berair yang digunakan di fasilitas kesehatan sering dikaitkan dengan infeksi yang didapat di rumah sakit. Meskipun pengolahan air dan klorinasi, air yang masuk ke sistem distribusi rumah sakit mungkin mengandung konsentrasi rendah dari berbagai mikroorganisme asli seperti Pseudomonas sp., Legionella sp., mikobakteri nontuberkulosis, Acinetobacter sp., Aeromonas sp., Sphingomonas sp., Enterobacter sp., Aspergillussp. dan amuba, yang dapat menyebabkan infeksi oportunistik yang penting secara klinis.
Tetap tertanam dalam matriks polimer organik ekstraseluler yang dikombinasikan dengan partikel nonorganik, mikroorganisme ini dapat mendorong pengembangan biofilm dalam sistem perpipaan fasilitas kesehatan, tangki air panas, menara pendingin AC, wastafel, kepala pancuran, dan aerator keran. Selain memiliki karakteristik masing-masing kelompok, biofilm merupakan penghalang, sehingga mencegah pembersihan lingkungan secara menyeluruh dan eliminasi total mikroorganisme, dengan konsekuensi adanya sisa-sisa yang, pada saat yang sama, dapat mengembangkan resistensi terhadap biosida dan menularkan resistensi ini, baik genetik, bahkan pada mikroorganisme spesies lain.
Beberapa bakteri pembentuk biofilm seperti Legionella, Klebsiella, Pantoea agglomerans, Acinetobacter baumannii dan Enterobacter cloacae dapat menyebabkan infeksi rumah sakit dan lebih resisten terhadap desinfektan dan antibiotik daripada keadaan planktoniknya. Biofilm dapat bertindak sebagai reservoir mikroba yang terus-menerus melepaskan mikroba yang layak ke dalam aliran air. Air keran kemudian dapat mencemari permukaan, peralatan dan instrumen medis serta endoskopi, mesin dialisis, nebulizer, pelembab udara dan ventilator (Exner et al. 2005 ).
Rute penularan patogen yang ditularkan melalui air termasuk kontak langsung, konsumsi air, kontak tidak langsung dan inhalasi bioaerosol. Pseudomonas aeruginosa dan Legionella pneumophila adalah patogen yang ditularkan melalui air yang paling signifikan di fasilitas kesehatan.
P. aeruginosa adalah mikroorganisme lingkungan umum. Hal ini sering dikaitkan dengan infeksi nosokomial, terutama di antara pasien dengan ventilasi mekanis atau pasien dengan gangguan sistem imun di unit perawatan intensif. Reservoir utama P. aeruginosa dianggap sebagai flora endogen pasien, dan transmisi horizontal di antara pasien telah lama dianggap sebagai sumber infeksi P. aeruginosa yang paling sering. Penelitian lain menunjukkan penyebaran pasien ke pasien melalui tangan petugas kesehatan, atau melalui fomites.
Namun, selama beberapa tahun terakhir, penerapan metode pengetikan molekuler memungkinkan untuk mengidentifikasi air ledeng yang dipasok oleh unit perawatan intensif sebagai sumber signifikan isolat P. aeruginosa eksogen. Sebuah tinjauan studi prospektif menunjukkan bahwa antara 14,2 dan 50% episode infeksi/kolonisasi pada pasien disebabkan oleh genotipe yang ditemukan di air unit perawatan intensif (Trautmann et al. 2005 ).
L. pneumophila telah diakui sebagai patogen pertama yang ditularkan melalui air yang ditularkan melalui inhalasi. Penularannya merupakan risiko yang cukup besar untuk pasien dengan penyakit paru-paru kronis dan mereka yang menjalani anestesi umum.
Di rumah sakit, status imunosupresif pasien dan faktor risiko lain menyebabkan tidak hanya risiko infeksi yang lebih tinggi tetapi juga insiden kematian yang lebih tinggi daripada di tempat lain. Dari 5 hingga 20% legionellosis yang dilaporkan berasal dari layanan kesehatan (Exner et al. 2005). Dalam pengaturan perawatan kesehatan, tidak hanya pelembab udara, alat pernapasan dan menara pendingin, tetapi juga pancuran dan keran adalah reservoir khusus Legionella (Joly dan Alary 1994 ; WHO 2007 ; ANSI/ASHRAE 2015 ).
Mikobakteri nontuberkulosis (NTM), bahkan disebut mikobakteri lingkungan, juga bertanggung jawab atas infeksi terkait perawatan kesehatan melalui rute inhalasi dan kontak langsung. Struktur dinding selnya sangat kaya akan lipid rantai panjang dan kemampuan untuk membentuk biofilm berkontribusi pada ketahanannya terhadap bahan kimia dan mendukung kegigihannya.
Memang, NTM sering ditemukan dalam sistem distribusi air dan dapat menjadi aerosol melalui pancuran dan keran. Sebuah survei mikrobiologi yang dilakukan oleh penulis mengkonfirmasi keberadaan NTM di pipa air rumah sakit setelah terjadinya beberapa kasus mikobakteriosis atipikal di bangsal rumah sakit. Beban NTM berkisar antara 2 × 10 2 dan 4 × 10 4 cfu/L dan spesies NMT oportunistik patogen manusia (M. intracellulare, M. chelonae, M. llatzerense dan M. gordonae ) ditemukan kecanduan spesies lingkungan tidak berbahaya lainnya (Briancesco et al. 2014 ).
Karena risiko yang dihasilkan dari keberadaan NTM dalam air tidak dapat dikendalikan oleh prosedur desinfeksi air klasik, filter pada titik penggunaan sekarang direkomendasikan untuk menjadi pilihan terbaik untuk meminimalkan risiko.
Selain itu, sistem distribusi air mungkin merupakan reservoir jamur dalam ruangan yang potensial seperti Aspergillus sp., zygomycetes, Fusarium sp. dan jamur lainnya. Hujan dan keran dapat menjadi sumber risiko aerosolisasi spora jamur (Anaissie et al. 2003). Jamur ada di mana-mana di alam dan tumbuh hampir di mana saja di dalam atau di luar ruangan.
Orang dapat terkena jamur melalui kontak kulit, menghirup atau menelan. Karena keberadaan jamur di lingkungan, beberapa tingkat paparan tidak dapat dihindari. Inhalasi biasanya dianggap sebagai mekanisme yang paling penting dari paparan jamur yang hidup (hidup) atau tidak hidup (mati), fragmen atau komponen jamur. Mayoritas spora jamur memiliki diameter aerodinamis 2-10 m, yang berada dalam kisaran ukuran yang memungkinkan partikel untuk disimpan di saluran pernapasan atas dan bawah. Paparan inhalasi spora jamur mengharuskan spora awalnya aerosol di tempat pertumbuhan. Secara umum, orang dengan gangguan pertahanan tubuh menderita jenis infeksi jamur yang paling parah.
Penyebaran Mikroorganisme di Udara
Mikroorganisme rumah sakit di udara tampaknya tidak berbahaya bagi orang sehat. Namun demikian, mereka dapat menyebabkan efek kesehatan yang merugikan pada individu immunocompromised.
Rumah sakit itu sendiri dan sistem teknologinya dapat menawarkan sumber yang merusak kualitas udara dalam ruangan. Sistem pendingin udara dan tanaman udara dapat terkontaminasi seiring waktu dan menjebak berbagai kontaminan seperti debu dan organisme biologis. Kelembaban dari mereka dapat mengembun di dalam saluran dan mendukung pertumbuhan mikroba. Oleh karena itu di rumah sakit, diperlukan penanganan dan ventilasi udara khusus untuk mencegah penularan melalui udara (ANSI/ASHRAE 2016 ). Ventilasi yang tidak memadai berimplikasi pada transmisi bakteri melalui udara (Obbard dan Fang 2003 ).
Bioaerosol menyebar melalui penutup udara dalam berbagai ukuran yang luas. Droplet lebih besar dari 5 m dan sumbernya terutama dari batuk, bersin atau berbicara. Di rumah sakit, pertunjukan medis tertentu seperti penyedotan dan bronkoskopi menyebarkan partikel sebesar ini. Di antara infeksi yang ditularkan melalui tetesan, cacar, campak, cacar air, TBC, penyakit meningokokus, pneumonia yang disebabkan oleh mikoplasma , SARS, dan flu adalah yang paling relevan.
Partikel kecil yang tersisa dari tetesan yang diuapkan (berukuran 5 m atau lebih kecil) dan partikel debu yang mengandung agen infeksi dapat tetap tersuspensi di udara untuk waktu yang lama. Dengan cara ini, mikroorganisme dapat tersebar luas oleh arus udara pada jarak yang lebih jauh dari sumbernya. Penularan infeksi melalui udara hanya melibatkan mikroorganisme yang menyebar dalam jumlah besar ke udara dengan dosis infektif yang rendah. Faktor kunci yang mempengaruhi tingkat beban mikroba di udara adalah kepadatan penghuni dan kelembaban tergantung pada lokasi tertentu di dalam rumah sakit.
Penelitian Mikrobioma di Rumah Sakit USA
hospitalmicrobiome – Jaringan Sains dan Inovasi Inggris UKUSA `Mengalahkan Superbug: Studi Mikrobioma Rumah Sakit untuk Mengatasi Resistensi Antimikroba` diadakan pada 14 Oktober 2013 di Departemen Kesehatan Inggris, London.
Lokakarya ini dirancang untuk mempromosikan kolaborasi ASInggris dalam studi mikrobioma rumah sakit untuk menambahkan segi baru pada pemahaman kolektif kita tentang resistensi antimikroba.
Penelitian Mikrobioma di Rumah Sakit USA – Para peneliti berkumpul memperdebatkan pentingnya komunitas mikroba rumah sakit dalam penularan penyakit dan sebagai reservoir untuk gen resistensi antimikroba, dan mendiskusikan metodologi, hipotesis, dan prioritas. Sejumlah pendekatan pelengkap dieksplorasi, meskipun pentingnya mikrobioma lingkungan yang dibangun dalam penularan penyakit tidak diterima secara universal.
Penelitian Mikrobioma di Rumah Sakit USA
Metode epidemiologi seluruh genom saat ini sedang dirintis di Inggris dan manfaat pindah ke analisis komunitas tidak selalu jelas bagi para perintis; namun, kemajuan pesat di bidang mikrobiologi lain menunjukkan kepada beberapa peneliti bahwa studi mikrobioma rumah sakit akan sangat bermanfaat bahkan dalam jangka pendek.Studi kolaboratif akan menggabungkan kembali kekuatan yang berbeda untuk mengatasi masalah internasional resistensi antimikroba dan infeksi terkait rumah sakit dan perawatan kesehatan.Studi kolaboratif akan menggabungkan kembali kekuatan yang berbeda untuk mengatasi masalah internasional resistensi antimikroba dan infeksi terkait rumah sakit dan perawatan kesehatan.Studi kolaboratif akan menggabungkan kembali kekuatan yang berbeda untuk mengatasi masalah internasional resistensi antimikroba dan infeksi terkait rumah sakit dan perawatan kesehatan.
Resistensi antimikroba (AMR) merupakan tantangan global dan biaya NHS diperkirakan £ 1 miliar per tahun, mempengaruhi puluhan ribu nyawa. Pada tahun 2013, para pemimpin G8 Igiris memimpin pernyataan bersama oleh Menteri Sains G8 di bulan penamaan prioritas AMR. Strategi Kesehatan / DEFRA Sarjana 5 Tahun untuk Mengatasi Konsensus AMR dalam Rilis Laporan Ancaman Resistensi Antibakteri oleh Pusat Pengendalian dan Pencegahan Penyakit.
Publikasi ini membuka jalan untuk mempercepat pengembangan kemoterapi antibakteri baru karena kedua negara berurusan dengan antibiotik yang ada. Di sisi lain, salah satu tempat paling penting untuk transmisi patogen resisten antibakteri adalah bidang medis. 5ri untuk semua pasien yang dirawat di fasilitas medis untuk didiagnosis dengan infeksi nosokomial. Infeksi ini menelan biaya sekitar $364,5 miliar ($ 2007) setiap tahun dan membunuh sekitar 100.000 orang. Melalui UK Research Councils, Wellcome Trust, dan National Institute for Health Research (NIHR), Inggris memiliki ancaman mikroorganisme terbesar: Staphylococcus aureus (MRSA) dan crostridium yang resistan terhadap methicillin. Studi-studi ini menampilkan penggunaan sekuensing seluruh genom yang berkelanjutan dalam layanan epidemiologi dan pengendalian infeksi.
Kemajuan yang sama dalam teknologi sekuensing yang memungkinkan epidemiologi seluruh genom juga memungkinkan karakterisasi filogenetik komunitas mikroba terbuka dan deteksi molekul tinggi gen resistensi antimikroba, pendekatan ortogonal untuk ekologi mikroba rumah sakit. Proyek Mikrobioma Rumah Sakit, yang dipimpin oleh Universitas Chicago, Institut Angkatan Darat Walter Reed, dan Layanan Terpadu Universitas Ilmu Kesehatan, membawa teknologi ini ke pendekatan ekologi komunitas untuk penyakit menular yang didiagnosis secara individual dan rumah sakit yang tidak terlibat langsung dalam penyakit menular tersebut. terintegrasi. Sehubungan dengan. kontrol.
Pendekatan ini merupakan penyimpangan yang signifikan dari strategi seluruh genom yang ada, yang secara sensitif memeriksa isolat bakteri atau virus klinis dan lingkungan yang dikultur yang menghadirkan minat khusus dan umumnya mengancam wabah nosokomial. Studi mikrobioma memberikan pengurangan karakterisasi galur individu sambil merangkul keragaman filogenetik yang lebih luas dari setiap sampel.
Studi mikrobioma di rumah sakit berusaha untuk mengkarakterisasi bakteri yang meningkatkan kesehatan dan penyebab penyakit di lingkungan rumah sakit, untuk memahami konsekuensi pembersihan, ventilasi, sterilisasi, dan penggunaan antibiotik profilaksis pada mikrobioma. Komunitas organisme di dalam rumah sakit penting karena beberapa alasan. Pertama, gen yang memberikan resistensi antibiotik ditemukan pada organisme non-patogen, bahkan di lingkungan abiotik yang paling tidak mungkin. Tentunya hal ini juga berlaku di lingkungan rumah sakit.
Baca Juga : Ekologi Mikroba di Lingkungan Buatan
Gen ini dapat ditransfer ke patogen dan membuat patogen baru yang resistan terhadap obat. Kedua, resistensi kolonisasi adalah karakteristik sebagian besar komunitas mikroba. Mekanismenya secara bertahap dijelaskan. Resistensi kolonisasi (utuh, terluka, atau dimanipulasi) mikroflora rumah sakit dapat berperan dalam pengendalian infeksi. Praktik pembersihan rumah sakit saat ini dan perawatan antibiotik tidak mempertimbangkan flora mikroba dan sebaliknya berfokus pada pengendalian mikroorganisme yang ditargetkan.
Menghancurkan atau menghancurkan ekologi mikroba rumah sakit melalui intervensi tersebut dapat mengurangi persaingan dengan organisme patogen dan meningkatkan kemampuan mereka untuk tumbuh dan menyebabkan penyakit. Akhirnya, efek promosi kesehatan atau probiotik dari organisme tertentu dan organisme tersebut dicirikan oleh kombinasi yang baik dalam lingkungan tertentu, seperti usus. Faktanya, obesitas telah terbukti berkorelasi dengan varian tertentu dari flora usus. Efek flora mikroba pada bangunan rumah sakit dan kesehatan pasien saat ini belum dipelajari dan berpotensi penting. Komponen lapangan Proyek Rumah Sakit Mikrobioma (HMP)dirancang untuk mengkarakterisasi komposisi taksonomi permukaan, udara, air, dan komunitas mikroba yang berhubungan dengan manusia di Universitas Chicago, Universitas Perawatan dan Penemuan (CCD). Lokakarya HMP pertama (78 Juni 2012) mengkaji strategi dan pendekatan pengambilan sampel awal untuk pengukuran bangunan, yang mengarah pada pengembangan proposal lengkap untuk Alfred P. Sloan, dan pendirian Rumah Sakit Konsorsium Mikrobioma. Workshop HMP ke2 (15 Januari 2013 diadakan segera sebelum dimulainya pengambilan sampel di CCD dan bertanggung jawab atas perubahan menit terakhir pada desain sampel dan penanganan sampel, serta berbagai aspek lain dari pelaksanaan proyek.
Di sini kami menyajikan diskusi dan kesimpulan dari lokakarya UKUSA UK Science and Innovation Network ‘Mengalahkan Superbug: Studi Mikrobioma Rumah Sakit untuk mengatasi Resistensi Antimikroba’, yang diadakan pada 14 Oktober 2013 di Departemen Kesehatan Inggris, London. Ini membawa keahlian dari Proyek Mikrobioma Rumah Sakit di AS ke Inggris, melalui dukungan dari Kantor Luar Negeri dan Persemakmuran Inggris, untuk berinteraksi dengan para ahli tentang AMR, penularan patogen, ilmu bangunan, kesehatan masyarakat, dll.
Dan untuk menentukan apa penelitian Inggris kelompok dapat berkontribusi pada lingkungan binaan dan penelitian mikrobioma terkait manusia? Ini juga merupakan kesempatan yang sangat baik untuk mengidentifikasi keprihatinan kritis dan saran yang berharga tentang bagaimana berbagai kelompok penelitian yang terkait dengan pemberantasan infeksi nosokomial dapat diintegrasikan dengan lebih baik. Akhirnya,agenda lokakarya disusun untuk memfasilitasi waktu diskusi yang maksimal mengenai nilai penelitian mikrobioma di lingkungan rumah sakit.
Ini diikuti dengan diskusi ekstensif tentang peluang pendanaan dan nilai melakukan penelitian ini di Inggris, dan diskusi ekstensif tentang nilai agenda penelitian ini, dan masalah potensial yang harus dipertimbangkan oleh proyek tersebut.dan peluang pendanaan. Ini diikuti dengan diskusi ekstensif tentang peluang pendanaan dan nilai melakukan penelitian ini di Inggris, dan diskusi ekstensif tentang nilai agenda penelitian ini, dan masalah potensial yang harus dipertimbangkan oleh proyek tersebut.
Ekologi Mikroba di Lingkungan Buatan
Ekologi Mikroba di Lingkungan Buatan – Mikroorganisme (makhluk hidup yang terlalu kecil untuk dilihat tanpa bantuan) ditemukan di setiap sudut bumi, dari bermil-mil di bawah permukaan hingga mata air panas yang mendidih hingga es Antartika. Juga disebut sebagai mikroba, mikroorganisme termasuk bakteri, jamur, dan virus yang sudah dikenal, serta beberapa jenis yang kurang dikenal.
Ekologi Mikroba di Lingkungan Buatan

hospitalmicrobiome – Ahli mikrobiologi memperkirakan bahwa ratusan juta spesies mikroba menghuni dunia kita, yang sebagian besar, paling-paling, kurang dipahami. Meskipun mikroba paling dikenal sebagai penyebab penyakit, mereka juga memainkan peran penting di hampir semua sistem fisik, mengubah kimia atmosfer, memungkinkan pencernaan pada organisme yang lebih besar, dan memecah bahan organik. Mikroba mempengaruhi siklus geokimia global dan tentu saja, membantu kita dalam pembuatan bir dan anggur.
Di lab, kami sering mempelajari satu jenis mikroba, “membiakkannya” dengan menumbuhkannya secara terpisah dalam cawan atau labu. Kultur adalah metode yang ampuh untuk memahami biologi satu jenis mikroba, memungkinkan banyak eksperimen terkontrol. Kultur juga memiliki keterbatasan.
Di alam, mikroba tidak hidup dalam isolasi, tetapi merupakan komponen komunitas dinamis yang kompleks, sering kali termasuk “makroorganisme” seperti tumbuhan dan hewan, juga. Komunitas mikroba ini berinteraksi dengan lingkungan mereka dalam berbagai cara, mempengaruhi, dan dipengaruhi oleh lingkungan mereka. Misalnya, lumut (sebenarnya komunitas alga dan jamur) perlahan-lahan mendegradasi batuan yang mereka huni melalui pelepasan asam karbonat.
Apa itu Ekologi Mikroba?
Bidang “ekologi mikroba” berusaha memahami bagaimana mikroba berinteraksi dengan organisme lain (termasuk makroorganisme dan mikroba lain) dan dengan lingkungan. Seperti lingkungan lainnya, bangunan dan benda buatan manusia lainnya menyediakan habitat yang kaya bagi mikroba. Bangunan menyediakan ruang dan nutrisi bagi mikroba, dan orang-orang (dan berbagai hewan dan tumbuhan) yang lewat terus-menerus membawa spesies baru ke komunitas.
Baca Juga : Mapping Mikroorganisme di Balik Infeksi
Secara tradisional, studi tentang mikroba di gedung-gedung telah difokuskan pada patogen yang diketahui atau pada mikroba yang dapat merusak struktur – hal-hal seperti jamur hitam di dinding, bakteri Legionella (dinamakan untuk wabah mematikan infeksi pernapasan yang disebabkannya pada konferensi American Legion) di air, dan patogen di udara. Para peneliti telah menekankan yang paling terlihat atau ganasagen yang terkait dengan wabah yang meluas atau paparan alergen.
Secara khusus mereka telah mencari hubungan antara keberadaan mikroba tertentu dan beberapa efek kesehatan yang terukur pada manusia. Mikroba ini sering dipelajari di laboratorium, di luar konteks di mana mereka menyebabkan masalah, dan tanpa memperhatikan komunitas dari mana mereka berasal. Organisme ini diisolasi dalam kultur dan dinilai hanya risikonya terhadap kesehatan manusia, atau membangun integritas. Ini bisa menjadi masalah karena perilaku banyak mikroba sangat bergantung pada organisme lain yang ada dalam suatu komunitas.
Mempelajari komunitas alami mikroba
Namun, studi mikroba di habitat asli mereka telah menantang karena berbagai alasan. Mikroba, menurut definisi, sulit untuk diamati secara langsung, dan pengamatan langsung dapat bernilai terbatas. Penampilan fisik mikroba umumnya bukan merupakan indikator yang berguna tentang apa mikroba itu (mikroba yang sangat berbeda dapat terlihat sangat, sangat mirip) atau potensinya untuk menyebabkan masalah (misalnya, bentuk bakteri patogen dapat terlihat identik dengan bentuk non patogen).
Dengan demikian, banyak peneliti menggunakan cara tidak langsung untuk mengkarakterisasi mikroba di habitat aslinya, misalnya dengan mempelajari produk sampingan dari aktivitas mikroba. Pada akhir 1980-an, Norm Pace dan rekan-rekannya memelopori pendekatan baru terhadap ekologi mikroba.
Para peneliti mulai meneliti mikroba di habitat aslinya dengan mengisolasi DNA atau RNA dari sampel lingkungan, dan mempelajarinya di laboratorium. Analisis DNA/RNA memungkinkan peneliti untuk memeriksa cara kerja mikroba, dan membuat kesimpulan yang lebih akurat tentang jenis mikroba yang ada di suatu lokasi serta potensi biologis (apa yang dapat mereka lakukan) dari mikroba tersebut.
Sejarah studi berbasis DNA/RNA
Pada 1980-an dan 1990-an, studi mikroba berbasis DNA dimulai, dan mengungkapkan detail menakjubkan tentang komunitas mikroba. Sebagai contoh, penelitian berbasis DNA menemukan bahwa ada lebih banyak jenis mikroba yang ada di sebagian besar sampel daripada yang dapat ditumbuhkan oleh siapa pun di laboratorium.
Dengan kata lain, sebagian besar jenis mikroba yang ada dalam sampel adalah “tidak berbudaya” dan pada dasarnya kami tidak tahu apa-apa tentang mereka. Studi berbasis DNA juga menyoroti skala besar keragaman mikroba – beberapa sampel (misalnya, beberapa gram tanah) mengandung ribuan spesies, yang sebagian besar belum pernah ditanam di laboratorium, atau dipelajari dengan cara apa pun.
Selama bertahun-tahun, fokus studi ekologi mikroba berbasis DNA adalah pada survei skala kecil dari jenis mikroba yang ada dalam sampel tertentu, karena keterbatasan dalam metode karakterisasi DNA. Survei skala besar (baik memeriksa banyak sampel atau mencirikan sampel individu secara mendalam) tidak pernah terdengar sebelumnya. Ini berubah dengan kemajuan teknologi pengurutan DNA, sebagian besar didorong oleh proyek “genom” seperti Proyek Genom Manusia , dan kegiatan terkait.
Sekuensing DNA melibatkan membaca urutan basa nukleotidaditemukan dalam potongan DNA tertentu. Proyek genom bertujuan untuk membaca seluruh “urutan” basa nukleotida untuk organisme tertentu. Inovasi teknologi yang didorong oleh program genom menyebabkan penurunan biaya secara eksponensial, dan peningkatan besar-besaran dalam kecepatan, pengurutan DNA.
Meskipun fokus umum dari orang-orang yang mengembangkan teknologi ini adalah pada manusia, teknologi tersebut dapat digunakan untuk sampel DNA apa pun, dan bantuan untuk bidang lain merupakan manfaat sampingan yang besar.
Sebuah revolusi dalam ekologi mikroba
Dengan demikian, pada tahun-tahun awal abad ke-21, sebuah revolusi baru dimulai dalam ekologi mikroba dengan penerapan sekuensing DNA berbiaya tinggi dan berbiaya rendah untuk mempelajari mikroba di lingkungan. Ini bahkan mengarah pada pendekatan umum baru yang disebut “metagenomik”, di mana seseorang mengambil sampel dari suatu lingkungan, mengumpulkan semua DNA yang ada, dan kemudian mengurutkan bagian-bagian dari DNA itu. Dengan pengurutan DNA yang murah, kami dapat mengurutkan lebih banyak dan lebih banyak lagi DNA lingkungan, dan mendekati sampel yang mewakili mikroba yang ada dalam sampel asli.
Dalam beberapa tahun terakhir, metagenomik, dan studi terkait komunitas mikroba telah dilakukan di berbagai ekosistem, dari lautan, sumber air panas mendidih, hingga “planet” tubuh manusia. Studi-studi ini mengubah pemahaman kita tentang ekosistem ini dan mengungkapkan tidak hanya “siapa yang ada” dalam sistem ini, tetapi juga membantu menentukan “apa yang mereka lakukan” di komunitas mereka. Kami telah menemukan enzim dan jalur biologis baru, mengukur kelimpahan alami relatif dari banyak spesies dan untuk pertama kalinya, telah mampu membandingkan komunitas mikroba yang berbeda dalam skala besar.
Meskipun sebagian besar studi awal berbasis DNA atau metagenomik komunitas mikroba berfokus pada apa yang disebut ekosistem “alami”, baru-baru ini, beberapa peneliti telah mengalihkan fokus ke lingkungan buatan. Hasil dari studi awal ini menarik, menunjukkan, misalnya, bahwa organisme yang ada di pancuran adalah bagian yang sangat berbeda, dan berpotensi mengkhawatirkan, dari organisme yang ada di sistem air kota.
Sloan Foundation dan microBEnet
Sejumlah laboratorium penelitian terlibat dalam pekerjaan “mikrobiologi lingkungan binaan” . Program Lingkungan Dalam Ruangan Yayasan Alfred P. Sloan mendanai sebagian dari pekerjaan ini dan mendukung pengembangan alat yang dapat diterapkan secara lebih luas di lingkungan dalam ruangan.
Sebagai bagian dari upayanya untuk memfasilitasi hubungan antara ahli ekologi mikroba dan ilmuwan udara dalam ruangan, Sloan Foundation mendanai proyek microBEnet . Dipimpin oleh Jonathan Eisen dari UC Davis dan Hal Levin dari Building Ecology Research Group, microBEnet mengumpulkan informasi tentang pekerjaan yang relevan dari penerima hibah Sloan, dan sumber daya lainnya, untuk mendorong pertukaran informasi antara dan di antara ahli ekologi mikroba dan ilmuwan udara dalam ruangan.
Mapping Mikroorganisme di Balik Infeksi
hospitalmicrobiome – Pada Januari 2013, saat University of Chicago bersiap untuk mengungkap gedung rumah sakit terbarunya, satu tugas terakhir tersisa: membersihkan sudut dan celah gedung, dari lantai ke furnitur hingga keran air.Orangorang yang melakukan swabbing adalah peneliti yang mengumpulkan sampel mikroorganisme—bakteri, jamur, dan virus yang pada dasarnya ada di manamana, termasuk di dalam dinding rumah sakit. Sebagai bagian dari inisiatif yang disebut Proyek Mikrobioma Rumah Sakit , para peneliti ini kembali ke rumah sakit sepanjang tahun untuk mengumpulkan hampir 12.400 sampel, dengan tujuan memetakan campuran mikroba yang mengisi lingkungan perawatan kesehatan.
Mapping Mikroorganisme di Balik Infeksi – Sama seperti usus manusia yang memiliki mikrobioma, begitu juga rumah sakit, tim tersebut mengemukakan. Mereka termasuk di antara kelompok peneliti yang berkembang yang percaya bahwa memahami komunitas ekologi mikroskopis rumah sakit dapat menjadi kunci untuk mencegah orang menjadi lebih sakit di rumah sakit ketika mereka seharusnya pulih. Mikrobioma usus kita telah dikaitkan dengan efek mulai dari penyakit Parkinson hingga respons imun tubuh ; beberapa ilmuwan percaya bahwa mikrobioma rumah sakit juga dapat berperan dalam kesehatan.Bukan rahasia lagi bahwa infeksi terkait perawatan kesehatan memiliki biaya kesehatan dan ekonomi yang besar.
Mapping Mikroorganisme di Balik Infeksi

Diperkirakan 440.000 infeksi terjadi setiap tahun di rumah sakit AS, menelan biaya hampir $ 10 miliar. Dan meskipun ada upaya untuk menjaga kebersihan gedung dan tangan serta peralatan pekerja, penyakit itu terus berlanjut. “Ada banyak penyakit inferior yang tidak dapat dijelaskan (sepsis, infeksi) yang terjadi di rumah sakit. Kami dapat mengidentifikasi bakteri yang paling terkait dengan kejadian ini, tetapi rincian infeksi mikroba di rumah sakit belum diketahui. Hmm.” Jack Gilbert, pemimpin Proyek Mikrobiologi Rumah Sakit dan ahli ekologi mikroba di Argonne National Laboratory.
Untuk menjawab pertanyaan ini, tim mengumpulkan sampel dari dua ruang perawatan dan beberapa lokasi di 10 kamar rumah sakit di gedung rumah sakit baru. Mereka membersihkan area ini sebelum gedung mulai menerima pasien dan pada tahun pertama setelah ruangan itu ditempati. Para peneliti mengambil sampel mikroba di udara rumah sakit dan di tubuh anggota staf; mereka juga mengumpulkan informasi lingkungan seperti kelembaban dan konsentrasi karbon dioksida untuk mengawasi jumlah penghuni manusia sepanjang siang dan malam. Sebagai komponen proyek yang terpisah, para peneliti mengukur variabel serupa di satu kamar pasien di rumah sakit Angkatan Darat AS di Jerman.
Itu bukan pemeriksaan pertama mikroorganisme yang hidup di gedunggedung. Pada tahun 1887, Thomas Carnelley menyelidiki kuman di udara di sekolah, selokan, dan rumah di Dundee, Skotlandia. Dan barubaru ini, tim peneliti lain memeriksa mikroba di unit perawatan intensif neonatal rumah sakit . Namun, proyek Chicago berskala lebih besar, sebagian dimungkinkan oleh kemajuan terbaru dalam teknologi pengurutan gen yang memfasilitasi pemrosesan banyak sekali sampel. Dan proyek ini adalah yang pertama tidak hanya untuk mengidentifikasi jenis mikroorganisme—ramah atau patogen—tinggal di rumah sakit, tetapi untuk mengukur bagaimana lokasi dan faktor lingkungan, seperti kelembaban, ventilasi, dan lalu lintas pejalan kaki, dapat membentuk populasi ini dari waktu ke waktu.
“Jika Anda dapat memahami pola komposisi komunitas mikroba dan bagaimana perubahan ini dari waktu ke waktu, Anda bisa mendapatkan ide yang cukup bagus tentang bagaimana mencegah beberapa transmisi organisme patogen,” kata John Chase, yang telah meneliti mikrobioma di Northern Arizona. Universitas dan tidak terlibat dalam Proyek Mikrobioma Rumah Sakit.
Misalnya, baik di usus atau di gedung, hanya sebagian kecil bakteri dalam mikroflora yang menimbulkan risiko infeksi. Sisanya adalah pengamat (kadang disebut penyusup) atau menguntungkan. Namun, banyak perawatan yang diterima pasien, seperti kemoterapi dan antibiotik, dapat mengubah campuran mikroorganisme ini, mengubah bakteri dan jamur yang umumnya tidak berbahaya menjadi patogen.
“Kami secara tradisional berasumsi bahwa satu-satunya organisme di rumah sakit adalah yang menyebabkan penyakit, dan jika terdeteksi, pasien berisiko terinfeksi,” kata Gilbert. .. “Tetapi data untuk mendukung ini sangat kurang.”
“Ketika Anda memasuki ruangan, Anda mengambil mikroba, dan ruangan mengambil mikroba dari Anda.”
Sebaliknya, infeksi nosokomial adalah bakteri “jahat”. mengatakan itu mungkin karena kehadirannya. Lagi pula, banyak orang yang bekerja di bidang medis tanpa sadar membawa patogen potensial ke sistem pencernaan dan kulit. Namun tidak seperti pasien yang lemah atau terganggu, mereka tidak jatuh sakit karena mereka dilindungi dari infeksi parah oleh sistem kekebalan mereka dan mikroba lain yang hidup di sana.
Baca Juga : Proyek Penelitian Mikroba
Hasil proyek belum dipublikasikan, tetapi Brent Stephens, Kolaborator Mikrobioma Rumah Sakit, mengungkapkan bahwa jenis bakteri tertentu yang biasa ditemukan pada kulit manusia, seperti beberapa spesies staphylococcus , streptococcus, dan corynebacterium , menjadi jauh lebih melimpah setelah rumah sakit. dibuka. Sementara itu, Pseudomonas , yang dapat menyebabkan infeksi kandung kemih, luka, dan paruparu, dan yang lebih jarang menjadi kolonisasi kulit, menjadi kurang banyak. Itu menunjukkan lingkungan rumah sakit dan manusia di dalamnya berbaur dengan cara yang mendorong pertukaran bakteri.
Ini sesuai dengan penelitian sebelumnya, yang telah menunjukkan bahwa manusia menyimpan dan memperoleh kenangkenangan mikroba dari bangunan melalui kulit. “Anehnya dengan cepat, ketika Anda memasuki sebuah ruangan, Anda mulai mengambil mikroba, dan ruangan itu mengambil mikroba dari Anda,” kata Daniel Freedberg, seorang ahli gastroenterologi dan asisten profesor kedokteran di Columbia University Medical Center di New York City.
Freedberg percaya peta mikrobioma rumah sakit—sesuatu yang menggambarkan permukaan tempat berkembang biaknya serangga tertentu—dapat memberikan wawasan berharga tentang kondisi lingkungan yang memungkinkan mikroba berkembang. Dia memimpin penelitian terbaru yang menunjukkan lingkungan rumah sakit memang bisa berperan dalam penularan infeksi . Penelitian tersebut mengaitkan pewarisan tempat tidur rumah sakit dari seorang pasien yang telah menerima antibiotik dengan risiko lebih tinggi terkena diare menular yang berpotensi mematikan yang disebabkan oleh clostridium difficile , bakteri yang sporanya tumbuh subur di usus manusia ketika bakteri normal telah dihancurkan oleh antibiotik.
Penelitian ini tidak mengidentifikasi alasan hubungan antara antibiotik dan infeksi, tetapi obat yang diterima oleh satu pasien mengubah pleksus usus, dan campuran serangga yang dimodifikasi ini diteruskan ke pasien berikutnya. Saya menunjukkan kemungkinan bahwa hal itu dilakukan . Predisposisi c untuk pasien kedua ini di tempat tidur. sulit . Atau, pasien dapat langsung menginfeksi pasien berikutnya dengan bakteri melalui kasur atau tempat tidur. Staf rumah sakit membersihkan tempat tidur di antara pasien, tetapi c. Spora sulit terkenal karena sulit dibunuh. (Di sisinya, Gilbert tidak yakin bahwa kebersihan saja dapat menghilangkan infeksi rumah sakit.) Kedua penjelasan tersebut menunjukkan efek dan metode mengubah flora usus dari satu pasien ke pasien lainnya.
Proyek Penelitian Mikroba
hospitalmicrobiome – Ahli biologi Daniel Smith, berjongkok di sebuah ruangan kosong di rumah sakit baru Universitas Chicago, menarik kapas putih di atas ubin yang berkilauan. Smith mempelajari ujung bernoda debu sebelum memecahnya menjadi tabung plastik berlabel “Tanah.”
“Ini sampel yang bagus untuk kita,” kata Smith, sambil memasukkan botol itu ke dalam kotak es kering. “Bahkan jika Anda tidak dapat melihatnya, ada miliaran sel (bakteri) di permukaan ini.” Dengan Smith di Argonne National Laboratory, ketika para ilmuwan mulai mengklasifikasikan kehidupan tumbuhan dan hewan berabad-abad yang lalu. Rekannya memulai penyelidikan serupa. Secara alami mikro.
Proyek Penelitian Mikroba – Tahun depan, mereka akan melacak peningkatan dan penurunan mikrobiota besar virus, jamur, dan mungkin bakteri terpenting di Rumah Sakit Wilderness, dan bagaimana mereka akan mempengaruhi kesehatan manusia di lingkungan yang membunuh sekitar 100.000 orang. Saya berencana untuk lebih baik memahami. Setiap tahun, dari penyakit menular yang didapat secara nasional. Upaya ini, yang dikenal sebagai Proyek Mikrobioma Rumah Sakit , mengikuti studi serupa tentang komunitas bakteri dalam tubuh manusia, di mana organisme uniseluler mengungguli sel manusia dengan 10 banding 1. Ini juga merupakan bagian dari bidang penelitian mikroba yang sedang berkembang yang didukung oleh penelitian terbaru. Kemajuan dalam biologi molekuler dan ilmu komputer telah membuat beberapa ilmuwan mempertanyakan apakah manusia adalah kekuatan paling kuat yang membentuk kehidupan manusia.
Proyek Penelitian Mikroba

Atau, seperti yang dikatakan ahli mikrobiologi Institut Teknologi California Sarkis Mazmanian, “Kita terdiri dari 90 persen bakteri.” DNA Anda. .. Beberapa di antaranya dikodekan dalam DNA bakteri kita,” kata Masmanian. “Jadi seberapa banyak tindakan kita berasal dari tindakan kita sendiri, bahkan bagaimana kita bekerja, dan mungkin bahkan dari apa yang kita pikirkan? Berapa banyak dari kita yang benar-benar manusia?
Bakteri sebagai Serangga
Sejak setidaknya 17 tahun, ilmuwan Belanda Antonie van Leeuwenhoek adalah ahli ekologi mikroba Argonne dan pemimpin upaya flora mikroba Institut, Too Easy World. Sebagian besar mikrobiota manusia, yang terdiri dari 10 hingga 100 triliun sel, ribuan spesies, dan setidaknya 8 juta gen endemik, tidak hanya tidak berbahaya, tetapi juga vital bagi kehidupan. Dengan memecah makanan, bakteri menghasilkan vitamin esensial, agen anti-inflamasi, dan senyawa yang meningkatkan metabolisme manusia.
Tetapi premis utamanya adalah bahwa mikroorganisme adalah musuh ekologis manusia yang ditakdirkan untuk dihancurkan. “Kami membandingkan bakteri dengan serangga kecil,” kata Gilbert dalam wawancara baru-baru ini di kampus Argonne yang luas dekat Lemont. “Penggunaan kata “kutu” untuk bakteri bermula dari ketakutan akan serangga kecil menyeramkan yang merayap di segala hal,” katanya.
Senjata perang mikroba (antibiotik, vaksin, sabun dan air biasa) telah menyelamatkan jutaan nyawa, dan Gilbert dan sejenisnya tidak menyarankan untuk menghentikan senjata penting seperti itu. .. Sebaliknya, misi mereka lebih halus. Dengan menyaring genom mikroba, mereka ingin mengungkap interaksi kompleks yang menguntungkan beberapa lanskap dan membuat yang lain lebih berbahaya.
Bagian dari pekerjaan ini didasarkan pada Proyek Mikrobioma Manusia, yang dimulai pada tahun 2007 untuk mengurutkan DNA mikroba pada orang sehat dan orang dengan berbagai kondisi seperti penyakit refluks gastroesofageal dan sindrom iritasi usus besar. Proyek, yang didanai oleh National Institutes of Health, menyimpulkan bahwa flora mikroba tertentu dikaitkan dengan atau mendahului penyakit tertentu.
“Ini bukan hanya mikroba di sisi lain manusia di sisi ini,” kata Rita Proctor, Koordinator Proyek NIH. “Ini membantu kita untuk memikirkan mikroorganisme sebagai berinteraksi satu sama lain dan dengan lingkungan, bukan sebagai entitas individu, tetapi sebagai bakteri atau patogen individu.”
Ekosistem manusia.
Para ilmuwan masih mendefinisikan hubungan, tetapi studi terbaru menunjukkan bahwa perubahan mikroba dapat mempengaruhi kesehatan dengan berbagai cara. Untuk menekankan hal ini, drg. Alexander Coles sering menyebut pasien dengan infeksi Clostridium difficile yang persisten pada tahun 2009. Setelah antibiotik membasmi bakteri normal, bakteri berbentuk batang biasanya tetap berada di usus besar. Jika dibiarkan, bakteri ini dapat menyebabkan diare, radang usus besar, dan kematian pada sekitar 14.000 kasus per tahun.
Pada saat pasien datang kepadanya, Khoruts mengatakan dia telah kehilangan lebih dari 60 pon dan berada di kursi roda. Khoruts, seorang ahli gastroenterologi di University of Minnesota Fairview, mengatakan: Ketika kesempatan habis, Khoruts menyarankan agar suami pasien memberikan sampel bakteri dari usus besar kepada istrinya. Segera setelah prosedur yang disebut transplantasi tinja , tes mengungkapkan bahwa pasien memiliki komposisi spesies bakteri yang berkembang biak di usus besar. Infeksi hilang. Transplantasi tinja tidak lagi didukung di bidang penelitian mikrobiota. Ini adalah bukti elegan tentang bagaimana mikrobiota usus mempengaruhi kesehatan. Tetapi hasil awal yang menarik telah muncul di seluruh spektrum ilmiah.
Misalnya, ketika para ilmuwan memberi tikus mikroba usus dari tikus gemuk, tikus penerima mengemas lebih banyak lemak. Dalam penelitian lain, tikus yang diberi molekul yang diproduksi oleh bakteri usus Bacteroides fragilis terlindungi dari penyakit seperti multiple sclerosis dan penyakit radang usus. Dan, dalam sebuah makalah 2011, para ilmuwan menemukan bahwa tikus bebas mikroba terlibat dalam perilaku berisiko daripada rekanrekan mereka yang sehat dan memiliki mikrobioma.
“Jika kita dapat memahami (mikrobioma),” kata Mazmanian, yang sedang menyelidiki bagaimana mikroba dapat meningkatkan sistem kekebalan tubuh. “Saya pikir kita bisa mendapatkan pijakan untuk memahami berbagai penyakit. Para ahli hidup dari penggunaan mikrobiota dan probiotik, atau apa yang diyakini bermanfaat bagi manusia. Penelitian bakteri memperingatkan bahwa itu masih sangat baru.
Meskipun klaim terkait dengan berbagai merek yogurt, para ilmuwan mencoba memahami dengan tepat bagaimana bakteri yang berbeda bekerja saat dicerna. Juga, sementara transplantasi tinja tampaknya efektif melawan beberapa infeksi, bakteri hidup tertentu sebenarnya dapat membahayakan pasien dengan kekebalan yang lemah.
“Masih sangat cepat,” kata Proctor. “Kami benar-benar di tingkat sensus. Dari sudut pandang biomedis, yang sebenarnya ingin kita ketahui adalah apa yang dilakukan mikroorganisme. Dan kapan Anda memiliki mikrobiota yang baik? Dan kapan flora mikroba kekurangan? Kami masih berjuang untuk mencari tahu bagaimana mengukurnya.
Zaman Manusia Mikroorganisme
Namun, semakin poly ilmuwan kini mencari jawaban atas pertanyaan-pertanyaan itu. Dari tempat kerja cadangannya pada Argonne, Gilbert memimpin Earth, Home, & proyek mikrobioma Rumah Sakit yg baru diluncurkan. Dia jua mempelopori upaya mikroba lainnya, mengeksplorasi apakah semprotan bakteri & produk lain bisa menaikkan output panen atau membantu tentara menutupi eksistensi mereka berdasarkan nyamuk.
“Ini merupakan abad mikroba,” istilah Gilbert, yg meluncurkan Proyek Mikrobioma Bumi dalam Juli 2010. Dorongan berdasarkan upaya tersebut, yg sang rekan-rekannya menggunakan hangat dipercaya sebagai “proyek akbar & gila”, merupakan buat mengidentifikasi & memilih fungsi seluruh mikroba Bumi, “buat kepentingan planet & umat insan.”
Dengan tahu mikroorganisme pada aneka macam lingkungan, Gilbert, 35, berharap bisa tahu berdasarkan mana berdari mikroba yg hayati dalam insan. “Anda nir bisa, secara harfiah, hanya mengisolasi insan & berkata, `Saya ingin memahami mengenai kesehatan insan,'” istilah Gilbert. “Anda wajib melihat lingkungan yg berinteraksi menggunakan insan.”
Namun, poly orang menghabiskan lebih poly ketika pada pada ruangan daripada pada luar ruangan. Jadi, Gilbert jua memulai Studi Mikrobioma Rumah, mengintip ke pos-pos mikroba pada tempat tinggal & apartemen, &, yg terbaru, Proyek Mikrobioma Rumah Sakit.
Selama 13 bulan ke depan, Daniel Smith & yg lainnya akan mengumpulkan kurang lebih 15.000 sampel berdasarkan 2 lantai teratas tempat tinggal sakit baru Universitas Chicago, Pusat Perawatan & Penemuan, yg dijadwalkan dibuka dalam Februari. Mereka akan menggesek penyeka steril pada lantai, konter, faucet & pasien & staf & mengumpulkan ratusan filter udara.
DNA mikroba akan dibawa ke lab Gilbert pada Argonne, pada mana para ilmuwan akan menjalankannya melalui mesin pengurutan kuat tinggi yg bisa membaca ratusan miliar pasangan basa – blok pembangun DNA – setiap beberapa hari. Hanya 5 tahun yg lalu, diharapkan lebih berdasarkan satu tahun buat melakukan jumlah pekerjaan yg sama, berdasarkan Gilbert.
Lari pendahuluan sudah memperlihatkan bahwa jenis bagian atas yg serupa mengandung bakteri yg serupa & bakteri yg tinggal pada tempat tinggal sakit secara teratur melompat ke sepatu pengunjung, yg lalu melacaknya pada luar.
Apakah itu baik, tidak baik atau bahkan relevan menggunakan kesehatan insan masih wajib dilihat. Namun menggunakan membentuk pengetahuan itu pada beberapa bulan & tahun mendatang, Gilbert ingin bisa menaruh liputan pada tempat tinggal sakit yg bisa dipakai buat mencegah infeksi tertentu, & dalam akhirnya, kematian terkait.
“Harapan kami,” istilah Gilbert, “merupakan bahwa data ini akan bisa memberi memahami kami bagaimana patogen terkait perawatan kesehatan memengaruhi orang-orang pada gedung-gedung ini & seberapa ad interim mereka, seberapa gigihnya mereka, & apa yg bisa kita lakukan buat menghentikannya. “
Permukaan dan Bakteriologi Udara Bangsal Terpilih di Rumah Sakit Rujukan, Ethiopia Barat Laut: Studi Cross-Sectional
hospitalmicrobiome – Lingkungan rumah sakit merupakan sumber patogen penting secara medis yang sebagian besar resisten terhadap berbagai obat (MDR) dan merupakan tantangan terapeutik utama. Tujuan dari penelitian ini adalah untuk menilai bakteriologi permukaan dan udara dari bangsal yang dipilih di Rumah Sakit Rujukan Felege Hiwot (FHRH), Northwest Ethiopia. Metode. Studi potong lintang dilakukan pada tanggal 15 Februari hingga 30 April 2017.
Permukaan dan Bakteriologi Udara Bangsal Terpilih di Rumah Sakit Rujukan, Ethiopia Barat Laut: Studi Cross-Sectional – Sebanyak 356 sampel permukaan dan udara diambil dari bangsal terpilih menggunakan agar darah domba 5% (Oxoid, UK) dan diproses di laboratorium mikrobiologi FHRH mengikuti standar bakteriologis. Prosedur. Isolat murni diuji terhadap antibiotik yang direkomendasikan menggunakan metode difusi cakram Kirby-Bauer, dan profil kerentanan ditentukan berdasarkan Clinical Laboratory Standards Institute (CLSI). Data dimasukkan dan dianalisis menggunakan SPSS versi 23 for Windows. Hasil . Dari total 356 sampel yang diproses, 274 berasal dari permukaan dan 82 dari udara.
Permukaan dan Bakteriologi Udara Bangsal Terpilih di Rumah Sakit Rujukan, Ethiopia Barat Laut: Studi Cross-Sectional
Di antaranya, 141 (39,6%) menunjukkan pertumbuhan bakteri, menghasilkan total 190 isolat. Isolat gram positif dominan pada 81,6% (), sedangkan gram negatif sebesar 18,4%. Isolat utama adalah staphylococci koagulase negatif ( CoNs ), 44%, diikuti oleh spesies S. aureus , 37,4%, dan Klebsiella sebesar 11,6%. Beban bakteri pada permukaan dan udara ditemukan di luar batas standar.
Selain itu, profil kerentanan antimikroba dari isolat menunjukkan bahwa sekitar 75% dari isolat yang diidentifikasi ditemukan resisten terhadap dua atau lebih agen antimikroba yang diuji. Kesimpulan. Studi ini menunjukkan tingkat beban bakteri yang tinggi yang melampaui batas standar pada sampel permukaan dan udara rumah sakit. Selanjutnya, sekitar 75% isolat ditemukan resisten terhadap berbagai obat. Oleh karena itu, penting untuk mengevaluasi dan memperkuat praktik pencegahan infeksi di rumah sakit. Selain itu, pemangku kepentingan juga harus memperkuat tindakan untuk mengurangi tekanan resistensi antimikroba di daerah yang diteliti.
1. Latar Belakang
Infeksi nosokomial (NIS) adalah infeksi yang diperoleh di unit rumah sakit atau layanan kesehatan yang muncul 48 jam atau lebih setelah masuk rumah sakit atau dalam waktu 3 hari setelah debit. Permukaan kontak tangan, lantai, dan udara di lingkungan rumah sakit merupakan sumber utama patogen berbeda yang dapat menyebabkan NIs. Sekitar 5% sampai 10% dari pasien yang dirawat di rumah sakit modern di negara-negara barat memperoleh satu atau lebih NI.
Sebaliknya, besarnya NI jauh lebih tinggi di negara berkembang karena alasan yang berbeda seperti sistem ventilasi yang buruk, debu yang tinggi, pengaturan yang terlalu padat, penyebaran melalui bersin dan batuk, pergerakan personel yang tinggi, dan pengelolaan lingkungan rumah sakit yang kurang optimal. Lingkungan rumah sakit merupakan reservoir penyebaran mikroba patogen tertinggi yang menimbulkan tantangan besar di lingkungan rumah sakit, terutama dalam hal NIS karena mengandung populasi mikroorganisme yang beragam .
Mikroorganisme seperti bakteri, jamur, dan virus dapat menyebabkan NIS. Laporan menunjukkan bahwa bakteri jauh lebih penting dalam hal ini. Organisme yang paling umum biasanya terkait dengan NIS adalah S. aureus , Cons , Pseudomonas aeruginosa , E. coli , spesies Klebsiella , dan spesies proteus yang bersumber dari pasien, tenaga kesehatan, petugas, instrumen yang terkontaminasi, dan lingkungan.
Sebagian besar strain bakteri di lingkungan layanan kesehatan adalah multidrug resistant (MDR). Penyebaran luas penggunaan obat, terutama atas atau penggunaan antibiotik yang tidak tepat, telah memberikan kontribusi untuk peningkatan insiden organisme resisten antimikroba, terutama di negara-negara berkembang .
Studi tentang kualitas bakteriologis bangsal fasilitas kesehatan di Ethiopia langka, dan beberapa yang tersedia melaporkan beban bakteri yang sangat tinggi. Secara nasional, pedoman pencegahan infeksi telah dikembangkan untuk fasilitas kesehatan di Ethiopia. Namun, kepatuhan penyedia layanan kesehatan terhadap protokol cukup terbatas yang dapat berperan dalam kualitas mikrobiologis yang buruk di berbagai fasilitas kesehatan .
Berdasarkan pengamatan kami, dalam setting penelitian ini, ada sejumlah mahasiswa ilmu kesehatan dan perdagangan pasien dan keluarga pasien yang tinggi di setiap bangsal FHRH. Selain itu, ada pembatasan yang buruk untuk masuknya individu yang tidak berwenang untuk mengakses unit rumah sakit yang berbeda. Banyak bangsal yang sangat kental dan tidak berventilasi baik.
Dengan latar belakang tersebut dan ketersediaan data yang cukup terbatas pada subjek di daerah penelitian, penelitian ini dilakukan untuk mengetahui tingkat kontaminasi bakteri dan profil kerentanannya terhadap antibiotik dari bangsal terpilih di Rumah Sakit Rujukan Felege Hiwot (FHRH) sebagai bagian dari layanan pencegahan infeksi. audit.
2. Bahan-bahan dan metode-metode
2.1. Setting Studi, Desain, dan Periode
Kami telah melakukan studi bakteriologi cross-sectional berbasis rumah sakit dari 15 Februari hingga 30 April 2017 di FHRH, Bahir Dar, Ethiopia Barat Laut. Kota Bahir Dar terletak sekitar 565 km dari Addis Ababa, ibu kota Ethiopia. FHRH didirikan pada tahun 1952 dan melayani lebih dari 10 juta orang Bahir Dar dan zona dan wilayah sekitarnya. Rumah sakit memiliki 13 bangsal, 430 tempat tidur, dan sekitar 531 tenaga kesehatan selama periode pengumpulan data. Klien rawat jalan harian lebih dari 600. Rumah sakit juga menampung mahasiswa kedokteran dan ilmu kesehatan lainnya dari Universitas Bahir Dar dan perguruan tinggi swasta untuk lampiran praktis.
Penulis melakukan observasional assessment di setiap bangsal selama periode pengambilan sampel untuk menilai kebersihan lingkungan, jumlah penghuni di setiap ruangan, penggunaan dan jenis desinfektan, situasi ventilasi, persiapan desinfektan, dan frekuensi pembersihan. Berdasarkan pengamatan kami, semua lantai bangsal dibersihkan dengan larutan yang mengandung pemutih tiga kali sehari.
Penyapuan kering dilakukan sebelum mengepel yang dapat menahan patogen di udara. Tidak ada sistem ventilasi mekanis di bangsal manapun. Hanya udara alami yang bersirkulasi di dalam ruangan yang dapat meningkatkan kemungkinan masuknya organisme dari lingkungan luar. Di semua bangsal, kami telah mengamati tidak ada praktik pembersihan rutin permukaan kontak tangan seperti dinding, kursi, tempat tidur, dudukan infus (IV), dan tandu. Sebaliknya, praktik pembersihan rutin di semua alat pelindung diri petugas kesehatan dipraktikkan. Namun, ada praktik yang buruk dalam melepas dan membuang alat pelindung diri sebelum meninggalkan kamar pasien.
2.2. Pengambilan Sampel dan Kultur Bakteriologis
Sebanyak 356 sampel bakteriologis permukaan dan udara dikumpulkan untuk analisis. Mempertimbangkan jumlah aliran pasien dan keselamatan pasien sakit kritis, lingkungan rumah sakit berikut dimasukkan untuk pengambilan sampel: Ruang Operasi (OT), bangsal bedah, unit perawatan intensif (ICU), unit perawatan intensif neonatal (NICU), dialisis dan kebidanan , bersalin, dan ortopedi. Area istirahat rumah sakit dikeluarkan.
Pengambilan sampel udara dilakukan dua kali sehari: pada pagi hari antara pukul 10 pagi hingga 11 pagi dan pada sore hari antara pukul 1 siang hingga 2 siang, dengan mempertimbangkan tingginya perdagangan manusia dalam interval waktu tersebut. Sampel dikumpulkan sesuai protokol standar menggunakan metode set plate atau metode passive air sampling mengikuti jadwal 1/1/1 (pada cawan petri steril berdiameter 90 mm yang mengandung 5% agar darah domba dibiarkan di udara selama 1 jam, 1 meter di atas lantai, dan 1 meter dari dinding). Selama prosedur pengambilan sampel udara, sarung tangan steril, masker bedah, dan gaun pelindung digunakan untuk mencegah kontaminasi pelat agar. Pelat diperiksa secara visual untuk setiap pertumbuhan bakteri sebelum digunakan.
Demikian pula, kapas steril yang dibasahi dengan salin normal steril digunakan untuk mengumpulkan sampel permukaan pada 1 cm x 1 cm·luas/cm 2 /permukaan seperti lantai, dinding, peralatan, instrumen, meja operasi, wastafel, sakelar lampu, kursi, tempat tidur, kain pasien, penangan pintu/loker, troli, tandu, wastafel/kran, dudukan infus, dan tabung oksigen . Semua jenis sampel diberi label dengan benar dan diangkut ke laboratorium Mikrobiologi FHRH dalam waktu 30 menit untuk analisis mikrobiologi.
Baca Juga : UChicago Medicine, Angkatan Darat AS Bergabung untuk Melatih Personil Perawatan Kesehatan Militer
Sampel udara dan permukaan diinokulasi pada pelat agar darah dan diinkubasi pada suhu 37°C selama 18-24 jam. Identifikasi isolat dilakukan berdasarkan prosedur standar mikrobiologi. Karakteristik koloni, reaksi gram, dan uji biokimia konvensional yang berbeda digunakan untuk mengidentifikasi isolat . Konsentrasi mikroba dari udara dinyatakan sebagai interims unit pembentuk koloni (CFUs) menggunakan colony counter, dan hasilnya dinyatakan dalam cfu / dm 2 / hr seperti yang dijelaskan sebelumnya. Demikian pula, hasil budaya swab dinyatakan dalam satuan pembentuk koloni menggunakan colony counter, dan hasilnya dinyatakan dalam cfu / cm 2.
2.3. Pengujian Kerentanan Antimikroba
Profil kerentanan antimikroba dari isolat dilakukan berdasarkan metode difusi cakram agar Kirby-Bauer. Suspensi organisme uji yang diidentifikasi dibuat dari koloni yang sama. Kepadatan suspensi ditentukan dengan membandingkan dengan larutan McFarland 0,5 Barium sulfat. Sebuah swab steril dicelupkan ke dalam suspensi isolat dalam kaldu dan kemudian dipercepat di seluruh permukaan pelat agar Muller-Hinton (Oxoid, LTD). Kemudian, disk antibiotik ditempatkan pada permukaan agar yang diinokulasi dan diinkubasi pada suhu 37°C selama 18-24 jam.
Diameter penghambatan pertumbuhan cakram diukur dan ditafsirkan sesuai dengan pedoman Clinical Laboratory Standards Institute (CLSI) [ 25]. Obat-obat diuji untuk kedua gram negatif dan gram positif yang ciprofloxacin (5 μ g), gentamisin (10 μ g), tetracycline (30 μ g), kotrimoksazol (25 μ g), kloramfenikol (30 μ g), ceftriaxone (30 μ g), norfloxacillin (10 μ g), dan Augmentin (30 μ g). Ampisilin (10 μ g) diuji hanya untuk negatif gram. Sebaliknya, penisilin (10 IU), eritromisin (15 μ g), cefoxtin (30 μ g), doksisiklin (30 μ g), klindamisin (2 μ g), dan klaritromisin (15 μ g) diuji untuk positif gram.
2.4. Analisis data
Semua data dimasukkan, dibersihkan, dan dianalisis menggunakan Paket Perangkat Lunak Statistik untuk Ilmu Sosial (SPSS) versi 23 (SPSS Inc., Chicago, IL, USA) untuk Windows. Data yang dihasilkan dikumpulkan dan disajikan dengan menggunakan statistik deskriptif.
2.5. Kontrol kualitas
Keandalan temuan studi dijamin melalui penerapan langkah-langkah pengendalian kualitas standar (QC) di seluruh proses pekerjaan laboratorium. Semua pelat kultur disiapkan sesuai dengan instruksi pabrik. Strain bakteri kontrol, seperti Escherichia coli (ATCC 25922), S. aureus (ATCC 25923), dan Pseudomonas aeruginosa (ATCC 27853), digunakan untuk memastikan kualitas cawan kultur dan cakram uji kepekaan antimikroba.
3. Hasil
3.1. Profil Bakteri Permukaan dan Udara
Sebanyak 356 sampel (274 permukaan dan 82 sampel udara) dianalisis, dimana beberapa 141 (39,6%) menunjukkan pertumbuhan bakteri menghasilkan total 190 isolat. Pertumbuhan campuran dilaporkan pada 42 (29,8%) sampel. Isolat gram positif mendominasi pada 155 (81,6%) diikuti oleh gram negatif, 35 (18,4%). Mayoritas bakteri yang diisolasi pada 102 (53,7%) ditemukan dari udara, dan sisanya pada 88 (46,3%) berasal dari permukaan.
3.2. Beban Bakteri dari Udara
Para penulis menentukan tingkat beban bakteri dari udara bangsal yang berbeda berdasarkan pendekatan yang direkomendasikan. Dari segi sebaran bangsal, jumlah isolat bakteri terbanyak diidentifikasi dari bangsal bedah sebesar 30,2% diikuti oleh bangsal bersalin sebesar 26,5%, ortopedi, dan NICU masing-masing sebesar 9,8%.
3.3. Beban Bakteri dari Permukaan
Rerata jumlah koloni aerobik (ACC) dari permukaan di rumah sakit lebih tinggi dari batas yang dapat diterima, di <5 cfu / cm 2. Rerata jumlah total koloni aerobik dari semua permukaan di bangsal diselidiki berada di 31,5 cfu / cm 2 . Rerata jumlah koloni bakteri tertinggi dilaporkan di bangsal bedah sebesar 48,8 cfu/cm 2 diikuti oleh bersalin, ortopedi, NICU, dan ICU sebesar 45,9 cfu/cm 2 , 34,9 cfu/cm 2 , 27,5 cfu/cm 2 , dan 16,5 cfu/ cm 2 , masing-masing, dan yang paling sedikit berada di PL pada 14,8 cfu/cm 2 . Tidak ada bakteri yang diisolasi dari ruang dialisis.
3.4. Profil Resistensi Antimikroba dari Isolat
Isolat gram positif, CoNs , menunjukkan tingkat resistensi yang tinggi terhadap penisilin, klaritromisin, dan eritromisin masing-masing sebesar 88%, 78,5%, dan 70,2%. Sebaliknya, isolat ini menunjukkan tingkat resistensi yang rendah terhadap klindamisin, amoksisilin/asam klavulanat, dan norfloksasilin masing-masing sebesar 17,2%, 19%, dan 22,6%.
4. Diskusi
Studi yang berbeda telah melaporkan bahwa permukaan kontak udara dan tangan unit layanan kesehatan terkontaminasi oleh patogen berbeda yang mungkin berfungsi sebagai sumber infeksi. Penelitian ini dilakukan untuk mendapatkan wawasan tentang distribusi, frekuensi, jumlah bakteri, dan profil kerentanan antimikroba patogen di pengaturan FHRH, yang merupakan salah satu rumah sakit tersibuk di Northwestern Ethiopia.
Hasil kultur aerobik mengungkapkan bahwa sekitar 141 (39,6%) permukaan dan sampel udara ditemukan terkontaminasi oleh berbagai bakteri patogen. Temuan ini relatif lebih rendah daripada penelitian serupa lainnya yang dilakukan di Ethiopia dan di luar negeri di Nigeria yang melaporkan pertumbuhan bakteri masing-masing sebesar 52,9% dan 65,7%.
Dalam penelitian ini, sekitar 81,6% isolat adalah gram positif yang sejalan dengan penelitian sebelumnya yang dilakukan di Rumah Sakit Ayder, Ethiopia, yang melaporkan 87,3%. Sebaliknya, distribusi lebih rendah dari positif gram di 43,1% dilaporkan di Hawassa, Ethiopia. Frekuensi gram positif yang lebih tinggi mungkin disebabkan oleh kondisi kering lingkungan rumah sakit dan penularan dari kulit, hidung, dan bisul dari petugas kesehatan dan pasien seperti yang dijelaskan sebelumnya.
UChicago Medicine, Angkatan Darat AS Bergabung untuk Melatih Personil Perawatan Kesehatan Militer
hospitalmicrobiome – Ahli bedah, perawat, dan petugas medis Angkatan Darat AS dilatih untuk memberikan perawatan yang menyelamatkan nyawa di garis depan, tetapi menjaga keterampilan itu agar tetap tajam dari medan perang bisa menjadi tantangan.
UChicago Medicine, Angkatan Darat AS Bergabung untuk Melatih Personil Perawatan Kesehatan Militer – Untuk membantu, Angkatan Darat AS telah bergabung dengan Pusat Medis Universitas Chicago untuk melatih personel perawatan kesehatan militer di pusat trauma Hyde Park sebelum penempatan mereka. “Hari ini menandai awal dari kemitraan unik yang akan memungkinkan anggota layanan aktif untuk meningkatkan dan mempertahankan keterampilan mereka untuk pengobatan medan perang sambil juga menyediakan sumber daya tambahan yang sangat dibutuhkan ke Sisi Selatan Chicago,” Ka Yee C. Lee, rektor Universitas Chicago, kata Kamis pagi.
UChicago Medicine, Angkatan Darat AS Bergabung untuk Melatih Personil Perawatan Kesehatan Militer

Mayor Jenderal Telita Crosland, wakil ahli bedah jenderal Komando Medis Angkatan Darat AS, mengatakan kemitraan itu penting untuk kemampuan anggota layanan untuk mempertahankan keahlian trauma mereka karena mereka akan bekerja di salah satu pusat trauma tersibuk di negara itu.
Tahun lalu, pusat trauma UChicago Medicine merawat 4.391 pasien dewasa dan anak-anak, meningkat 47% dari 2019, menurut staf universitas. Dari sekitar 3.800 pasien dewasa yang dirawat, 57% mengalami luka trauma tumpul akibat insiden seperti kecelakaan mobil dan jatuh, sementara 41% lainnya mengalami luka trauma tembus akibat penembakan atau penusukan.
Dr Kenneth Wilson, direktur medis pusat trauma UChicago Medicine dan ahli bedah militer di US Army Reserves, adalah kekuatan pendorong di balik kemitraan baru. Wilson, yang telah melayani beberapa penempatan di Irak dan Afghanistan, mengatakan pelatihan trauma penting untuk kesiapan medan perang.
“Ketika Anda berada di instalasi militer sebagai anggota tim medis, Anda tidak melakukan banyak perawatan trauma setiap hari. Rumah sakit militer terutama menyediakan layanan perawatan kesehatan untuk populasi muda yang sehat, jadi jarang ada jenis cedera yang Anda lihat di pusat trauma sipil yang sibuk yang secara teratur merawat orang-orang yang pernah mengalami kecelakaan atau penembakan dengan kecepatan tinggi, ” kata Wilson dalam sebuah pernyataan. “Jadi, ini bisa menjadi kurva pembelajaran yang curam untuk beralih dari lingkungan semacam itu ke suatu tempat seperti Suriah. Rumah sakit seperti UChicago Medicine menyediakan jalan tengah yang ideal yang memungkinkan tim berlatih bersama, membangun ‘memori otot’ mereka dan menjaga keterampilan mereka tetap segar.”
Diluncurkan pada tahun 2019, program Pelatihan Tim Trauma Militer-Sipil Departemen Kedokteran Angkatan Darat (AMCT3) beroperasi di tujuh pusat trauma yang sibuk di seluruh negeri, termasuk Pusat Medis Universitas Vanderbilt dan Pusat Medis Universitas North Carolina.
UChicago Medicine dipilih untuk berpartisipasi dalam program tersebut karena memiliki “saus rahasia” memiliki beban kerja yang tepat, hubungan dan kemauan untuk bekerja dengan Angkatan Darat, menurut Crosland. Sementara fokus utamanya adalah “mempertahankan keterampilan medis individu, (kemitraan) adalah peluang luar biasa untuk bekerja sebagai tim yang merawat pasien yang menderita trauma dan sakit kritis,” kata Crosland.
Kelompok 20 anggota pertama dokter Angkatan Darat dijadwalkan mulai tiba musim gugur ini di UChicago Medicine dari Fort Bragg di North Carolina. Personel medis Angkatan Darat akan bertugas dalam tugas rotasi jangka pendek atau ditempatkan di UChicago Medicine di mana mereka akan bekerja sebagai staf penuh waktu hingga tiga tahun.
Letnan Kolonel Timothy Plackett, seorang ahli bedah trauma, datang lebih dulu dari kelompok dan telah bekerja di UChicago Medicine sejak Januari. Plackett mengatakan program ini bermanfaat bagi dokter Angkatan Darat, rumah sakit, dan masyarakat karena anggota layanan dan staf rumah sakit saling belajar.
“Kami belajar praktik terbaik dari satu sama lain dan menggunakan apa yang telah dipelajari di Irak dan Afghanistan untuk secara langsung mengubah perawatan yang kami berikan di South Side,” kata Plackett dalam sebuah pernyataan. “Dan perawatan yang akan kami berikan di South Side akan secara langsung mengubah perawatan yang dapat kami berikan saat tim kami dikerahkan.” Pada akhirnya, sebanyak 30 personel medis Angkatan Darat akan berlatih di Chicago setiap tahun, termasuk ahli bedah, dokter pengobatan darurat, perawat, petugas medis tempur, ahli anestesi, dan lain-lain.