Perubahan Ekologi Mikrobioma Saluran Pernapasan dan Pneumonia Nosokomial
Pneumonia nosokomial merupakan salah satu infeksi yang paling sering terjadi pada pasien kritis.
hospitalmicrobiome – Hal ini terutama terkait dengan ventilasi mekanis yang menyebabkan penyakit parah, kematian yang tinggi, dan rawat inap yang berkepanjangan. Risiko kematian telah meningkat dari waktu ke waktu karena meningkatnya infeksi bakteri multidrug-resistant (MDR), yang merupakan ancaman kesehatan masyarakat global. Penelitian microbiome saluran pernapasan (RTM) sedang berkembang, dan penelitian terbaru menunjukkan bahwa RTM yang sehat secara positif merangsang sistem kekebalan tubuh dan, seperti mikrobioma usus, dapat melindungi terhadap infeksi patogen melalui resistensi kolonisasi (CR).
Perubahan Ekologi Mikrobioma Saluran Pernapasan dan Pneumonia Nosokomial – Kondisi fisiologis pasien kritis dan intervensi seperti pemberian antibiotik dan ventilasi mekanis secara dramatis mengubah RTM, menyebabkan disbiosis. Disbiosis RTM pasien ICU mendukung kolonisasi oleh patogen oportunistik dan resisten yang dapat menjadi bagian dari mikrobiota atau diperoleh dari lingkungan rumah sakit (biotik atau buatan). Meskipun bukti terbaru menunjukkan pentingnya RTM pada infeksi nosokomial, sebagian besar interaksi host-RTM tetap tidak diketahui. Dalam konteks ini, kami menyajikan perspektif kami mengenai penelitian di RTM yang mengubah ekologi di lingkungan klinis, terutama sebagai risiko untuk mendapatkan pneumonia nosokomial. Kami juga merefleksikan kesenjangan di lapangan dan menyarankan arah penelitian di masa depan. Selain itu, intervensi berbasis mikrobioma yang diharapkan bersama dengan alat untuk mempelajari RTM yang menyoroti pendekatan “omics” juga dibahas.
Perubahan Ekologi Mikrobioma Saluran Pernapasan dan Pneumonia Nosokomial

Saluran pernapasan adalah sistem organ yang berjalan dari lubang hidung ke alveoli paru-paru. Ini dibagi menjadi saluran pernapasan supratoraks (atas) (URT) dan saluran pernapasan intratoraks (bawah) (LRT) dengan permukaan sekitar 100 meter persegi . Selama bertahun-tahun, beberapa penelitian telah mengungkapkan keberadaan ekosistem mikroba residen yang menghuni permukaan saluran napas: mikrobioma saluran pernapasan (RTM), sangat padat di URT. Sebagai mikrobioma gastrointestinal (GIM), RTM merupakan ekosistem berkelanjutan dengan gradien longitudinal dan transversal keragaman mikroba dari rongga hidung dan mulut ke alveoli . Namun, RTM dan GIM berbeda dalam biomassa, keanekaragaman dan komposisi taksonomi.
Pada individu yang sehat, kompleksitas dan biomassa GIM meningkat dari lambung ke usus besar, mencapai 10 10 -10 12 CFUs/mL . Pada RTM, orofaring memiliki densitas bakteri yang tinggi (10 7 -10 8 CFU/ml), namun saat berpindah dari mulut ke paru-paru terjadi penurunan progresif, mencapai 10 4 -10 5 sel bakteri per mL alveolus. cairan intraluminal. Komposisi RTM dipengaruhi oleh kondisi pertumbuhan mikrobiologi lokal yang ditentukan oleh ketersediaan nutrisi, mikro-geografi, dan kondisi fisikokimia seperti eskalator mukosiliar, tekanan oksigen, aliran darah, pH, suhu, interaksi sistem kekebalan manusia, dan faktor lingkungan . Sumber utama mikroorganisme RTM adalah orofaring, yang akhirnya bermigrasi ke LRT melalui mikroaspirasi dan dispersi mukosa .
Model ekologi RTM saat ini dikenal sebagai “model pulau paru-paru yang diadaptasi” , dan menyerupai proses biogeografi, yang diturunkan dari model keseimbangan yang diusulkan oleh MacArthur dan Wilson (1963) dari biogeografi pulau . “Model yang disesuaikan” menunjukkan bahwa kekayaan mikroba dalam RTM didasarkan pada keseimbangan imigrasi (ekstensi mukosa, aspirasi mikro) dan eliminasi (pembersihan silia, batuk, mekanisme kekebalan antimikroba) spesies ke paru-paru dari URT. Pada dasarnya, struktur RTM tergantung pada laju migrasi stokastik, pertumbuhan, kepunahan, dan penyebaran epidemi anggota komunitas mikroba, proses yang dipengaruhi oleh faktor anatomi, fisiologis, dan klinis . Model ini akan membantu menjelaskan gradien keragaman mikroba, biomassa, dan penurunan kompleksitas dari rongga mulut ke paru-paru. Dickson dan rekan menyatakan bahwa, dalam kesehatan, mikrobioma paru-paru lebih dipengaruhi oleh imigrasi dan eliminasi mikroba daripada oleh kondisi pertumbuhan lokal. Namun, kondisi pertumbuhan lokal lebih kritis selama penyakit klinis lanjut. Model ekologi berbasis mikrobioma ini memberikan kerangka teoretis untuk infeksi patogen, lebih akurat daripada pandangan tradisional tentang pneumonia berdasarkan pertumbuhan cepat penyerang ke paru-paru steril.
Komposisi bakteri RTM yang sehat terutama terdiri dari Firmicutes, Bacteroidetes, dan Proteobacteria, yang merupakan tiga dari empat filum utama di semua mikrobioma spesifik lokasi manusia. Genera yang paling melimpah adalah Streptococcus, Prevotella , atau Veillonella , yang juga mendominasi dalam mikrobioma oral. Hanya beberapa penelitian yang mengkarakterisasi anggota RTM lainnya sebagai jamur, archaea, atau virus. Dengan kemungkinan pengecualian Saccharomycetes (sebagai genus Candida) di orofaring, sulit untuk memastikan apakah pada tingkat yang lebih rendah (sub-trakea) ada “mikobioma pernapasan” yang normal, jika jamur yang ditemukan di RTM sesuai dengan jamur lingkungan yang dihirup, atau jika sebagian dari mereka lebih sedikit.
rentan terhadap pembersihan fisiologis. Mycobiome pernapasan yang sehat diperkaya dengan jamur lingkungan dari filum Ascomycota dan Basidiomycota, yang paling umum juga di GIT. Banyak jamur sesuai dengan Eremothecium, Systenostrema, genus Cladosporium, dan keluarga Davidiellaceae yang, bersama dengan Saccharomycetes, juga merupakan taksa yang paling umum di GIT. Virome LRT sebagian besar masih belum dijelajahi, terutama pada orang sehat. Meskipun demikian, mirip dengan virom usus, virus eukariotik dan banyak bakteriofag telah dijelaskan dalam penelitian yang berbeda. Beberapa penelitian menunjukkan fungsi virom pernapasan dalam priming dan modulasi respon imun inang, serta kontrol spesies mikroba lain di dalam paru-paru.
Faktor-faktor yang membentuk keragaman virom tetap tidak diketahui, meskipun komposisinya di saluran pernapasan tampaknya ditentukan oleh kesehatan inang dan keberadaan populasi bakteri tertentu di bronkus, seperti yang telah disarankan pada cystic fibrosis . Sebuah studi metagenomik dari virome setelah transplantasi paru-paru berdasarkan sampel allograft bronchoalveolar lavage (BAL) menunjukkan bahwa saluran pernapasan penerima transplantasi paru-paru diperkaya dalam populasi kompleks anellovirus. Viral load juga telah berkorelasi dengan dysbiosis bakteri yang mempengaruhi hasil transplantasi dan menunjukkan bahwa interaksi virus-bakteri sangat penting untuk keseimbangan sistem mikrobioma-imun dan, dengan demikian, untuk fisiologinya.
Baca Juga : Agenda Penelitian untuk Mikrobiologi Dalam Ruangan, Kesehatan Manusia, dan Bangunan
Selain itu, kelimpahan bakteriofag yang tinggi di RTM layak untuk penelitian mendalam untuk menentukan apakah mereka memainkan peran yang sama seperti yang diamati di GIM, yaitu, mengendalikan homeostasis mikroba (mekar, komposisi mikroba, keragaman, metabolisme, dan memfasilitasi transfer gen horizontal ( HGT).Arkaea metanogenik telah terdeteksi di mikrobioma hidung, GIT, kulit, dan paru-paru, dan filum Woesearchaeota tampaknya berasosiasi dengan paru-paru. Namun, selain beberapa studi deskriptif, fungsi fraksi non-bakteri dari RTM layak untuk dianalisis lebih lanjut.
Ekologi RTM adalah bidang penelitian yang muncul yang mendapatkan perhatian karena beberapa penelitian menunjukkan peran menguntungkan dari penghuni mikroba dalam stimulasi sistem kekebalan dan perlindungan terhadap patogen (resistensi kolonisasi, CR), seperti yang telah didokumentasikan secara luas untuk mikrobioma usus. Homeostasis mikrobioma dapat terganggu sementara, misalnya, oleh penggunaan antibiotik, penggunaan peralatan medis (intubasi, ventilator), kejadian abnormal sementara (aspirasi), atau penyakit tertentu (penyakit virus dapat mengurangi efektivitas eskalator pembersihan bronkus) yang memungkinkan beberapa patogen untuk tumbuh terlalu cepat dan meningkatkan kolonisasi dan, pada akhirnya menyebabkan infeksi di LRT.
Sebagian besar penelitian yang terkait dengan RTM fokus pada penyakit pernapasan kronis tertentu seperti: B. Populasi mikroba yang mengkolonisasi paru-paru dengan cystic fibrosis. Pada penyakit ini, hiperviskositas saluran napas mendorong pertumbuhan multibakteri dan disbiosis di sepanjang saluran udara. Bakteri yang paling sering dikaitkan dengan kolonisasi kronis cystic fibrosis adalah Pseudomonas aeruginosa, Staphylococcus aureus, Stenotrophomonas maltophilia, Burkholderia, dan Pandoraea, yang sering berkolonisasi. Namun, ada juga mikroorganisme yang berhubungan dengan rongga mulut seperti actinomycetes, fusobacteria, gemella, granuricatella, neisseria, porphyromonas, prevotella, Russia, streptococcus, hemophilus, dan veillonella. Menariknya, pada pasien dengan cystic fibrosis, bakteri pemangsa RTMLRT seperti Bdellovibrio dan Bampirovibrio, serta parasit dari bakteri Parcubacteria phylumr TMS, ditemukan dalam memerangi populasi bakteri patogen.
Di sini, kami menyajikan perspektif kami mengenai penelitian dalam ekologi RTM yang berubah di lingkungan klinis, meningkatkan kemungkinan untuk memperoleh pneumonia nosokomial di area rumah sakit berisiko tinggi sebagai ICU, dan mendiskusikan kemajuan terbaru pada topik tersebut. Kami juga membahas kesenjangan di lapangan, masa depan intervensi berbasis mikrobioma untuk mencegah dan mengobati pneumonia nosokomial, dan kontribusi pendekatan “omics” untuk memahami peran dinamika RTM dalam timbulnya infeksi pernapasan.
Ekologi Mikrobioma Pernapasan pada Pneumonia Nosokomial
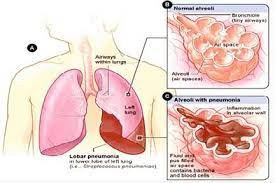
Infeksi LRT akut, pneumonia atau eksaserbasi bronkitis kronis, adalah penyebab utama mortalitas dan morbiditas di seluruh dunia. Pada orang tua, perkembangan pneumonia terjadi cepat, dengan prognosis buruk, terutama terkait dengan rawat inap, dan angka kematian yang tinggi sering di ICU. Pneumonia nosokomial, infeksi alveolus paru yang sebagian besar disebabkan oleh bakteri, tetapi juga virus, atau jamur terdiri dari pneumonia yang didapat di rumah sakit dan terkait ventilator dan merupakan masalah kesehatan masyarakat yang signifikan karena sering disebabkan oleh patogen yang resistan terhadap banyak obat (MDR) yang didapat di dalam paru-paru. lingkungan rumah sakit.
Pneumonia terkait ventilator merupakan penyebab pertama infeksi nosokomial pada pasien dengan ventilasi mekanik dan kedua tersering di unit perawatan intensif (ICU), dengan infeksi jangka panjang yang sering disebabkan oleh bakteri MDR. Skenario ini telah memburuk selama pandemi COVID-19 karena peningkatan dramatis dalam infeksi sekunder SARS-CoV-2 dan penggunaan antibiotik yang berlebihan, yang menyebabkan peningkatan yang luar biasa dari infeksi MDR dan transmisi gen resistensi antibiotik (ARGs). Kontribusi mikrobioma terhadap respons imun bawaan dan adaptif menunjukkan bahwa mikrobioma yang sehat dapat menjadi faktor yang berkontribusi terhadap rasio kematian kasus yang lebih rendah dari COVID-19. Di sisi lain, disbiosis mikrobioma dapat dikaitkan dengan respons imun yang buruk dan hasil penyakit yang lebih buruk. Bidang ini baru dan studi yang tersedia mengenai mikrobioma COVID-19 telah melaporkan hasil yang kontradiktif.
Salah satu faktor yang menyebabkan kontradiksi tampaknya menjadi perancu seperti ventilasi mekanis pada pasien ICU, mengubah struktur komunitas RTM, termasuk banyaknya taksa oral yang sebelumnya terkait dengan COVID-19. Studi pengambilan sampel paru-paru yang terinfeksi secara langsung melalui bronkoskopi telah terbukti paling akurat sejauh ini untuk mengidentifikasi tanda tangan mikrobiologis dan imunologis alveolar yang terkait dengan infeksi SARS-CoV-2. Sebuah penelitian berdasarkan 142 pasien yang menjalani bronkoskopi menunjukkan bahwa hasil klinis sebagian dapat dijelaskan oleh kelimpahan virus alveolar, dan kolonisasi oleh bakteri turunan mikrobioma URT ( Mycoplasma salivarium ), dan respons imun adaptif yang buruk.
Model ekologi pneumonia mengusulkan bahwa keseimbangan RTM dipindahkan ke keadaan disbiosis yang ditandai dengan keragaman mikroba yang rendah, beban mikroba yang tinggi, dan respons inflamasi inang. Apakah disbiosis adalah penyebab atau efek dari penyakit pneumonia masih belum jelas. Faktanya, peran dan dinamika mikrobioma RTM pada pasien kritis hampir tidak diselidiki, dan oleh karena itu intervensi yang diarahkan mikrobioma belum dimasukkan dalam pedoman klinis. Tentu saja, gangguan RTM dapat dipengaruhi oleh keadaan fisiologis yang mengubah ekologi lokal, termasuk: (1) peradangan, perubahan profil metabolit, dan mekanisme pertahanan lokal yang melemah oleh infeksi (yaitu, virus), mendukung migrasi dan pertumbuhan stokastik bakteri ; (2) komposisi kimia abnormal dari bronkus, seperti pada cystic fibrosis ; (3) kelainan anatomi dan kondisi lain yang menyebabkan obstruksi, seperti pada bronkiektasis, cystic fibrosis, penyakit paru obstruktif kronik, edema paru (yang dapat menjadi sekunder untuk sepsis), atau kanker paru-paru; (4) kondisi berbahaya eksternal, seperti paparan jangka panjang terhadap dingin, yang menyebabkan vasokonstriksi mukosa pada mukosa saluran pernapasan dan penekanan respons imun, atau pemicu alergi untuk asma; (5) peningkatan migrasi bakteri (yaitu, aspirasi menyeluruh cairan lambung, perubahan mikrobioma oral, intubasi, ketidaksadaran, posisi terlentang), dan penurunan proses eliminasi (tidak sadar, intubasi, obat penenang, kepala terangkat, gangguan pembersihan mukosiliar) ; (6) penyakit yang mendasari dan intervensi medis (yaitu, imunosupresi terapeutik, intubasi, ventilasi mekanis, atau terapi antibiotik jangka panjang) yang mendukung kolonisasi patogen oportunistik.
Pneumonia nosokomial dapat bersifat endogen, yang disebabkan oleh patogen oportunistik seperti Streptococcus pneumoniae atau Haemophilus influenzae , yang merupakan bagian dari RTM manusia yang sehat. Pneumonia ini umumnya muncul segera setelah masuk. Namun, kasus perkembangan pneumonia yang terlambat sering melibatkan patogen MDR yang didapat di rumah sakit, termasuk P. aeruginosa , Enterobacteriaceae yang memproduksi extended spectrum beta lactamases (ESBL), dan/atau carbapenemases, dan Methicillin-resistant Staphylococcus aureus (MRSA), yang sering diseleksi dan tersebar di lingkungan ICU. Pandangan patogen-sentris penyakit menular baru-baru ini bergerak ke arah perspektif ekologis berdasarkan interaksi host-patogen-mikrobioma-lingkungan. Dalam konteks ini, pneumonia nosokomial mewakili skenario kompleks di mana beberapa faktor mungkin berperan dalam timbulnya dan hasil infeksi.